��Ŀ����
����Ŀ������������� 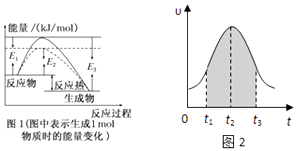
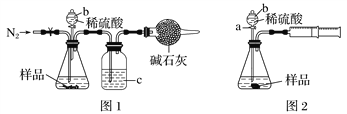
��1������ͼ1��д���ϳɰ����Ȼ�ѧ����ʽ��������E1��E2��E3��ʾ����
��2��ʵ����0.01mol/L��KMnO4��������Һ��0.1mol/L��H2C2O4��Һ�������Ϻ�Ӧ���ʦ�[mol/��Ls��]�뷴Ӧʱ��t��s���Ĺ�ϵ��ͼ2��ʾ���÷�Ӧ�Ļ�ѧ����ʽΪ��2KMnO4+5H2C2O4+3H2SO4�TK2SO4+2MnSO4+10CO2��+8H2O���ش��������⣺
��0��t2ʱ����ڷ�Ӧ���������ԭ���ǣ� ��
��t2��tʱ����ڷ�Ӧ���ʼ�С��ԭ���ǣ� ��
��ͼ����Ӱ���֡��������ʾt1��t3ʱ���� ��
A��Mn2+���ʵ���Ũ�ȵ����� B��Mn2+���ʵ���������
C��SO42�����ʵ���Ũ�� D��MnO4�����ʵ���Ũ�ȵļ�С��
���𰸡�
��1��N2��g��+3H2��g��?2NH3��g����H=��2��E3��E1��kJ/mol
��2����Ӧ�в�����Mn2+�����Ǵ˷�Ӧ�Ĵ���������ʹ��Ӧ���������Ӱ����ڷ�Ӧ��Ũ�ȼ�Сʹ��Ӧ���ʼ�С��Ӱ�죻���ŷ�Ӧ�Ľ��У���Ӧ��Ũ����С����ΪӰ�췴Ӧ���ʵ���Ҫ���أ��Ӷ���Ӧ���ʼ�С��AD
���������⣺��1����ͼ��֪�÷�ӦΪ���ȷ�Ӧ��������1mol������ų�������Ϊ��E3��E1��kg��������2mol���������Ϊ2��E3��E1��kg�����÷�Ӧ���Ȼ�ѧ����ʽΪN2��g��+3H2��g��2NH3��g����H=��2��E3��E1��kg/mol��
���Դ��ǣ�N2��g��+3H2��g��2NH3��g����H=��2��E3��E1�� kJ/mol����2�������ŷ�Ӧ�Ľ��У�Ũ����С������������˵����Ӧ�в�����Mn2+�����Ǵ˷�Ӧ�Ĵ���������ʹ��Ӧ���������Ӱ����ڷ�Ӧ��Ũ�ȼ�Сʹ��Ӧ���ʼ�С��Ӱ�죬
���Դ��ǣ���Ӧ�в�����Mn2+�����Ǵ˷�Ӧ�Ĵ���������ʹ��Ӧ���������Ӱ����ڷ�Ӧ��Ũ�ȼ�Сʹ��Ӧ���ʼ�С��Ӱ�죻�����ŷ�Ӧ�Ľ��У���Ӧ���Ũ�Ƚ��ͣ�Ũ��Խ�ͣ���Ӧ����ԽС������Ũ�ȵĸı��Ƿ�Ӧ���ʱ仯����Ҫԭ��
���Դ��ǣ����ŷ�Ӧ�Ľ��У���Ӧ��Ũ����С����ΪӰ�췴Ӧ���ʵ���Ҫ���أ��Ӷ���Ӧ���ʼ�С���۸���v= ![]() ���Ƶ���v����t=��C��������Ӱ�����ʾ��Ӧ��Ũ�ȵļ��ٻ�������Ũ�ȵ����ӣ���ѡAD��
���Ƶ���v����t=��C��������Ӱ�����ʾ��Ӧ��Ũ�ȵļ��ٻ�������Ũ�ȵ����ӣ���ѡAD��