��Ŀ����
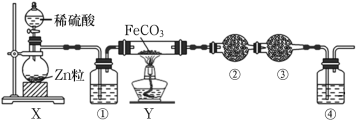
����Ŀ��ʵ�������������������������з�����ȡ�ģ��Իش��������⣺
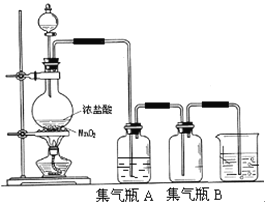
��1������װ���еķ�Ӧ�Ļ�ѧ����ʽ___����������ԭ��Ӧ��___�������������ԭ��Ӧ����ָ��___����������___�ǻ�ԭ����
��2������ƿA��ʢװ���DZ���ʳ��ˮ��ע�������ڱ���ʳ��ˮ���ܽ�Ⱥ�С�����Ȼ����ڱ���ʳ��ˮ�е��ܽ����ܴ���������__��
��3����������ˮ�����ԣ��������ж������о��ҵĴ̼��ԣ�������������������ж���������������β��ֱ����������У�����Ⱦ������ʵ�����пɲ���__��Һ�������ж���������
��4��һ��ʵ���У���Ũ����800mL�����ܶ�Ϊ1.19g��cm-3��HCl����������Ϊ36.5%����һ������MnO2��ַ�Ӧ��������5.6L��STP�����������Լ���Ũ��������ʵ���Ũ�Ⱥͱ�������HCl�����ʵ���___��___��
���𰸡�4HCl��Ũ��+MnO2![]() Cl2��+MnCl2+2H2O �� MnO2 HCl ��ȥ�����л��е�HCl���� Ũ�������ƣ�Ũ� 11.9mol/L 0.5mol
Cl2��+MnCl2+2H2O �� MnO2 HCl ��ȥ�����л��е�HCl���� Ũ�������ƣ�Ũ� 11.9mol/L 0.5mol
��������
��1�����ݻ�ѧ��Ӧ��Ԫ�صĻ��ϼ۱仯������������Ԫ�ػ��ϼ����ߵ�����Ϊ��ԭ����
��2�����������ڱ���ʳ��ˮ���ܽ�Ⱥ�С�����Ȼ����ڱ���ʳ��ˮ�е��ܽ�Ⱥܴ���������
��3��������������Ӧ������β���Ĵ�����
��4������c=![]() ������Ũ�ȣ�������������ԭ��Ӧ��֪������1mol����������2mol��HCl�����������㡣
������Ũ�ȣ�������������ԭ��Ӧ��֪������1mol����������2mol��HCl�����������㡣
��1���ڷ�Ӧ4HCl��Ũ��+MnO2![]() Cl2��+MnCl2+2H2O�У�MnԪ�صĻ��ϼ���+4�۽���Ϊ+2�ۣ���MnO2Ϊ��������ClԪ�صĻ��ϼ���-1�����ߵ�0����HClΪ��ԭ�����ʴ�Ϊ��4HCl��Ũ��+MnO2
Cl2��+MnCl2+2H2O�У�MnԪ�صĻ��ϼ���+4�۽���Ϊ+2�ۣ���MnO2Ϊ��������ClԪ�صĻ��ϼ���-1�����ߵ�0����HClΪ��ԭ�����ʴ�Ϊ��4HCl��Ũ��+MnO2![]() Cl2��+MnCl2+2H2O���ǣ�MnO2��HCl��
Cl2��+MnCl2+2H2O���ǣ�MnO2��HCl��
��2���������ڱ���ʳ��ˮ���ܽ�Ⱥ�С�����Ȼ����ڱ���ʳ��ˮ�е��ܽ�Ⱥܴ���Ũ�����ӷ���ʹ���ɵ������л���HCl����ʳ��ˮ������Ϊ��ȥ�����л��е�HCl���壬
�ʴ�Ϊ����ȥ�����л��е�HCl���壻
��3���������ж��������ŷ��ڻ����У��������ܱ������գ��������Ũ�������ƣ�Ũ�������β����
�ʴ�Ϊ��Ũ�������ƣ�Ũ���
��4��Ũ����800mL�����ܶ�Ϊ1.19gcm-3��HCl����������Ϊ36.5%����Ũ��������ʵ���Ũ����c=![]() =
=![]() =11.9mol/L��
=11.9mol/L��
��4HCl��Ũ��+MnO2![]() Cl2��+MnCl2+2H2O��֪���������������1mol�������ɣ�����2mol��HCl��������
Cl2��+MnCl2+2H2O��֪���������������1mol�������ɣ�����2mol��HCl��������
��������HCl�����ʵ���Ϊ![]() ��2=0.5mol��
��2=0.5mol��
�� 11.9mol/L��0.5mol��

 �Ͻ�ƽСѧ��������ϵ�д�
�Ͻ�ƽСѧ��������ϵ�д� �Ƹ������������ϵ�д�
�Ƹ������������ϵ�д�����Ŀ������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ����
|
|
|
|
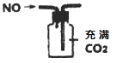
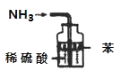
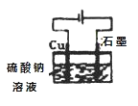
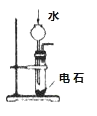
A����ͼ��ʾװ�ã����ţ����ռ�NO���� | B����ͼ��ʾװ�ÿ����ն��ఱ�����ܷ�ֹ���� | C����ͼ��ʾװ�ÿ�ʵ�ַ�Ӧ��Cu+2H2O | D����ͼ��ʾװ�ÿ�ʵ������Ȳ |
A. AB. BC. CD. D