题目内容
(12分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血
剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图(标出电极材料和电解质溶液),并写出电极反应式。

正极反应 ,
负投反应 。
(3)某同学用碳棒、铜棒和稀硫酸为原材料,以及一些必要条件,实现 Cu+H2SO4(稀)=CuSO4+H2↑反应。请在框内画出能够实现这一反应的实验装置图。

(4)另一位同学在做(3)反应实验时,看到碳棒和铜棒
上都有气泡产生,但铜棒没有被腐蚀。请你分析其原因
,
此时的总反应为 。
剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式 。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图(标出电极材料和电解质溶液),并写出电极反应式。

正极反应 ,
负投反应 。
(3)某同学用碳棒、铜棒和稀硫酸为原材料,以及一些必要条件,实现 Cu+H2SO4(稀)=CuSO4+H2↑反应。请在框内画出能够实现这一反应的实验装置图。

(4)另一位同学在做(3)反应实验时,看到碳棒和铜棒
上都有气泡产生,但铜棒没有被腐蚀。请你分析其原因
,
此时的总反应为 。
(12分)(1)2Fe3++Cu=2Fe2++Cu2+(2分)
(2)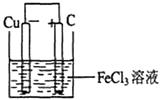 (2分)
(2分)
正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)
负极反应:Cu=2Cu2++2e-(或Cu-2e-=Cu2+)(2分)

(3)(2分,无直流电源不给分)
(4)电源反接了,2H2O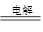 H2↑+O2↑(4分)
H2↑+O2↑(4分)
(2)
 (2分)
(2分)正极反应:Fe3++e-=Fe2+(或2Fe3++2e-=2Fe2+)
负极反应:Cu=2Cu2++2e-(或Cu-2e-=Cu2+)(2分)

(3)(2分,无直流电源不给分)
(4)电源反接了,2H2O
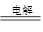 H2↑+O2↑(4分)
H2↑+O2↑(4分)略

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
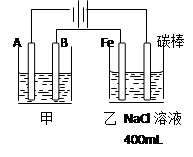
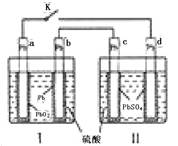
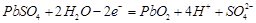
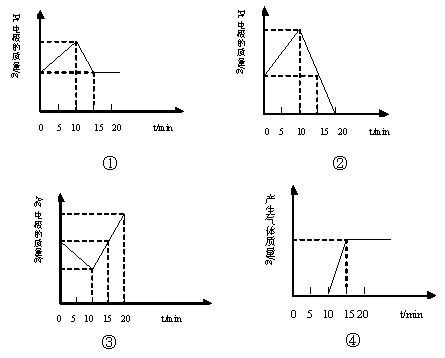
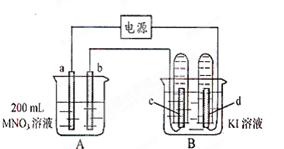

 。电解进行一段时
。电解进行一段时 也收集到了气体,此时c极上的电极反应式为: 。
也收集到了气体,此时c极上的电极反应式为: 。 溶液的物质的量浓度为 mol·L-1。
溶液的物质的量浓度为 mol·L-1。