题目内容
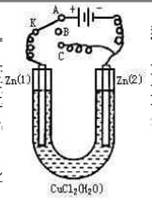
将质量相等的银片和铂片分别作为阳极和阴极用来电解硝酸银溶液
i.以电流强度为1A通电10分钟;
ii.10min后,反接电源,以电流强度为2A继续通电10分钟;下列图像分别表示:银电极质量,铂电极质量,及电解池产生气体质量和电解时间的关系图。下确的是( )
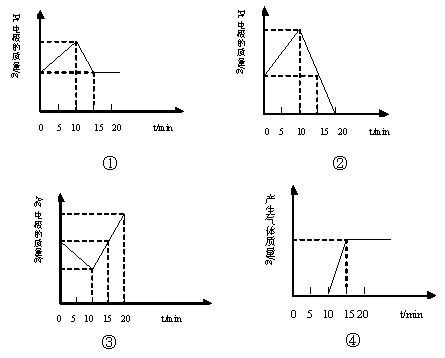
i.以电流强度为1A通电10分钟;
ii.10min后,反接电源,以电流强度为2A继续通电10分钟;下列图像分别表示:银电极质量,铂电极质量,及电解池产生气体质量和电解时间的关系图。下确的是( )

| A.①③ | B.①②③ | C.②③④ | D.①②③④ |
A
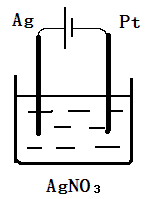
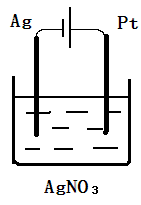
i ii
i和ii均为电解池,所用材料不变,只是电源反接。
i. 阳极(Ag):Ag - e- = Ag+ 银电极质量减少
阴极(Pt): Ag+ + e- = Ag 有银在铂电极析出,质量增加
i过程通过1A电流10min
ii. 10min - 15min 阳极(Pt):Ag - e- = Ag+ 铂电极质量减少
阴极(Ag): Ag+ + e- = Ag 有银在银电极析出,质量增加
这个过程中通过2A电流5min,与i过程电流一样多,完全时i过程的逆过程,所以此过程中铂电极减少的质量与i过程增加的质量一样,银电极增加的质量与铂电极减少的质量一样。
15min-20min 阳极(Pt):4OH- - 4e- = O2↑+ 2H2O 电极质量不变,有气体生成
阴极(Ag):Ag+ + e- = Ag 电极质量继续增加
所以,Pt电极质量变化为①,Ag电极质量变化为③,产生气体的质量应从15min开始到20min一直增加,然后不变,所以④不对。

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目


 +2e
+2e =2H
=2H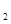 ↑
↑