题目内容
【题目】常温下,下列有关电解质溶液叙述错误的是
A. 某H2SO4溶液中c(OH-)/c(H+)=1.0×10-8,由水电离出的c(H+)=1×10-11mol·L-1
B. 将0.02mol·L-1盐酸与0.02mol·L-1Ba(OH)2溶液等体积混合后溶液pH约为12
C. 将一定体积稀盐酸与稀氨水混合,当溶质为NH3·H2O和NH4Cl时,溶液的pH一定大于7
D. 向0.1mol·L-1Na2CO3溶液中逐滴滴加0.1mol·L-1稀盐酸,溶液中c(HCO)先增大后减小
【答案】C
【解析】
A. 由水电离出的c(H+)等于由水电离出的c(OH-);
B.根据混合后得到的溶液中c(OH-)浓度来计算;
C. 将一定体积稀盐酸与稀氨水混合,当溶质为NH3·H2O和NH4Cl时,溶液的pH可能小于或等于7;
A项,由![]() =1.0×10-8,c(OH-)
=1.0×10-8,c(OH-)![]() c(H+)=1
c(H+)=1![]() 10-14可得c(OH-)=1×10-11mol·L-1,所以由水电离的c(H+)=1×10-11mol·L-1,故A项正确;
10-14可得c(OH-)=1×10-11mol·L-1,所以由水电离的c(H+)=1×10-11mol·L-1,故A项正确;
B项,假设体积均为1L,等体积混合后体积为2L,反应后剩余OH-的物质的量为0.02mol,得到c(OH-)=1×10-2mol·L-1,溶液pH约为12,故B项正确;
C项,将稀盐酸与稀氨水混合,随着盐酸量的增加,NH4Cl浓度增加,NH3·H2O浓度减小,溶液可以显酸性,中性或者碱性,故C项错误;
D项,向0.1mol·L-1Na2CO3溶液中逐滴滴加0.1mol·L-1稀盐酸,随着盐酸量的增大,先生成HCO3―,而后HCO3―与盐酸反应生成二氧化碳,故溶液中c(HCO3―)先增大后减小,故D项正确。
综上所述,本题正确答案为C。

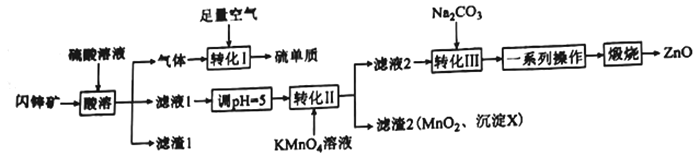
【题目】工业上以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为:Na2Cr2O7·2H2O),其主要工艺流程如下:

查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42-,自身被还原为Bi(OH)3固体。
ii.几种金属离子沉淀的pH:
物质 | 开始沉淀的pH | 完全沉淀的pH |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.4 | 4.4 |
Cr(OH)3 | 4.6 | 5.9 |
Fe(OH)2 | 7.5 | 9.7 |
Bi(OH)3 | 0.7 | 4.5 |
回答下列问题:
(1)加入过量硫酸之前先要将铬铁矿矿石粉碎,其目的是________________________。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和___________(填仪器名称)。
(3)写出④反应的化学方程式_____________________________________________。
(4)⑤中酸化是使CrO42-转化为Cr2O72-![]() 写出该反应的离子方程式_____________。
写出该反应的离子方程式_____________。
(5)将溶液H经下列操作:蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
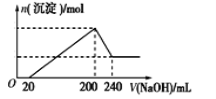
(6)取一定质量的固体D溶解于200 mL的稀硫酸中,向所得溶液中加入5.0 mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为_________,固体D中含铁化合物的物质的量为___________。