题目内容
(1)某溶液中Cl-、Br-、I-的物质的量之比为2:3:4,要使溶液中的Cl-、Br-、I-的物质的量之比变为4:3:2,则通入Cl2的物质的量与原溶液中I-的物质的量之比为 .
(2)要使溶液中只有Cl-和Br-,而没有I-,则此时Cl-和Br-的物质的量之比为 .
(3)若要使溶液中只有Cl-,则通入Cl2的物质的量和原溶液中Br-的物质的量之比为 .
(2)要使溶液中只有Cl-和Br-,而没有I-,则此时Cl-和Br-的物质的量之比为
(3)若要使溶液中只有Cl-,则通入Cl2的物质的量和原溶液中Br-的物质的量之比为
考点:化学方程式的有关计算
专题:计算题
分析:(1)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,由反应可知,溶液中离子总物质的量不变,故溶液中Br-离子物质的量不变,再利用赋值法,结合离子的物质的量的变化计算;
(2)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,要使溶液中只有Cl-和Br-,而没有I-,可能是碘离子恰好完全反应或者是溴离子部分反应;
(3)设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,若要使溶液中只有Cl-,根据得失电子守恒,则通入Cl2的物质的量为
mol.
(2)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,要使溶液中只有Cl-和Br-,而没有I-,可能是碘离子恰好完全反应或者是溴离子部分反应;
(3)设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,若要使溶液中只有Cl-,根据得失电子守恒,则通入Cl2的物质的量为
| 7x |
| 2 |
解答:
解:(1)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,由反应后离子物质的量关系可知反应离子的物质的量分别为4xmol、3xmol、2xmol,则Cl-的物质的量增加2xmol,I-的物质的量减少2xmol,则通入氯气xmol,则通入Cl2物质的量与原溶液中I-物质的量之比为x:4x=1:4,即为1:4,
故答案为:1:4;
(2)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,要使溶液中只有Cl-和Br-,而没有I-,可能是碘离子恰好完全反应时需氯气的量为:2xmol氯气,生成4xmolCl-,此时溶液中氯离子的物质的量为6xmol;溴离子恰好完全反应需要氯气
mol,此时溶液中的氯离子为9xmol;所以则此时Cl-和Br-的物质的量之比为2≤
<3,故答案为:2≤
<3;
(3)设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,若要使溶液中只有Cl-,根据得失电子守恒,则通入Cl2的物质的量为
mol,通入Cl2的物质的量和原溶液中Br-的物质的量之比为7:6,故答案为:7:6.
故答案为:1:4;
(2)离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,要使溶液中只有Cl-和Br-,而没有I-,可能是碘离子恰好完全反应时需氯气的量为:2xmol氯气,生成4xmolCl-,此时溶液中氯离子的物质的量为6xmol;溴离子恰好完全反应需要氯气
| 7x |
| 2 |
| n(Cl-) |
| n(Br-) |
| n(Cl-) |
| n(Br-) |
(3)设原溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,若要使溶液中只有Cl-,根据得失电子守恒,则通入Cl2的物质的量为
| 7x |
| 2 |
点评:本题考查氧化还原反应的计算,题目难度不大,本题注意把握离子的还原性强弱,判断发生的反应是关键,在根据反应的离子方程式计算.

练习册系列答案
相关题目
下列试剂中,不能贮存在玻璃瓶中的是( )
| A、浓硫酸 | B、氢氟酸 |
| C、浓氢氧化钠溶液 | D、硝酸银溶液 |
A、B为短周期元素,A元素原子的L层比B元素原子的L层少2个电子,B元素原子核外电子数比A元素原子核外电子总数多4个,则A、B两元素形成的化合物可表示为( )
| A、BA |
| B、BA2 |
| C、B2A2 |
| D、A2B2 |
在40g密度为d g/cm3的硫酸铁溶液中,含有1.4g Fe3+离子,则此溶液中Fe3+的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各组物质不能按“→”所示关系实现转化的是(“→”表示反应一步完成)( )
A、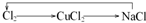 |
B、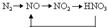 |
| C、S→SO2→H2SO4→MgSO4 |
| D、Al→Al2O3→Al(OH)3→NaAlO2 |