题目内容
以下大小关系不正确的是
| A.熔点:Na>Mg | B.硬度:金刚石>晶体硅 |
| C.键能:H—F>H—Cl | D.晶格能:NaF>NaCl |
A
解析试题分析:A.熔点:Na<Mg,错误;B.由于共价键C—C>Si—Si,所以硬度:金刚石>晶体硅,正确;C.元素的非金属性越强,元素的原子与H原子形成的共价键就越强,所以键能就越大。由于非金属性F>Cl,所以键能:H—F>H—Cl。正确;D.离子间的键长越短,键能越大,晶格能就越大,由于离子键Na—F>Na—Cl,则晶格能:NaF>NaCl,正确。
考点:考查微粒之间的作用力及熔沸点、硬度等性质的比较的知识。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案(15分)W、M、N、X、Y、Z是六种常见的短周期元素,其原子半径随原子序数的变化如右图所示,已知W的一种同位素的质量数为18,中子数为10;M和Ne原子的核外电子数相差1;N与X相邻,N的单质是日常生活中常用的金属材料;Y的最外层电子数是其最内层电子数的3倍;Z的非金属性在同周期主族元素中最强。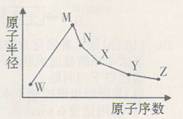
(1)W的另一种同位素的质子数与中子数相等,原子符号表示为 ;元素Y在周期表中的位置是 。
(2)下列有关物质性质的比较中,正确的是 (填字母编号)。
| A.W、X、Y三种元素最简单氢化物的稳定性:W>Y>X |
| B.M、X、Z三种元素形成的单质熔点:X>M>Z |
| C.Y、Z两种元素的含氧酸酸性:Z>Y |
| D.Y、Z两种元素的单核阴离子还原性:Y>Z |
(4)元素X与Z形成的五原子分子的空间结构属于 形。
(5)与Z同族的元素都能与氢元素形成氢化物,其中水溶液酸性最弱的是 (填化学式)。
(6)含有N元素的两种离子在溶液中相遇能快速发生反应,写出该反应的离子方程式 。
某学生在做元素性质与原子结构关系的实验时,设计了一套实验方案,并记录了有关的实验现象。请帮助该学生整理并完成实验报告。
(1)实验目的
探究同一主族元素性质的递变规律。
(2)实验用品
仪器:试管、胶头滴管
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳
(3)实验内容(在下表横线中填写相关内容)
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈_____色 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈_____色 |
(4)实验结论:_________________________________。
(5)问题和讨论
①上述两个实验中发生反应的离子方程式分别为________________、__________________。
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:______________、______________。
下列说法正确的是
| A.碘化铵和氯化铵受热分解过程中破坏和形成的化学键类型完全相同 |
| B.反应N2H4(l)=N2(g)+2H2(g)是一个△S>0的反应 |
| C.1 mol FeCl3完全水解得到的Fe(OH)3胶体中胶粒数目为NA(NA为阿伏加德罗常数) |
| D.HClO是弱酸,所以NaClO是弱电解质 |
在以离子键为主的化学键中常含有共价键的成分。下列各组原子形成化学键中共价键成分最少的是( )
| A.Li,F | B.Na,Cl | C.Na,F | D.Mg,O |
下列变化过程中,只破坏共价键的是( )
| A.I2升华 | B.NaCl颗粒被粉碎 |
| C.HCl溶于水得盐酸 | D.从NH4HCO3中闻到了刺激性气味 |
下列物质中,中心原子的杂化类型为sp3杂化的是
| A.C2H6 | B.C2H2 | C.BF3 | D.C2H4 |
下列说法正确的是
| A.由分子构成的物质一定含有共价键 |
| B.由非金属元素组成的化合物不一定是共价化合物 |
| C.非极性键只存在于双原子单质分子中 |
| D.不同元素组成的多原子分子中的化学键一定都是极性键 |
下列各组物质中化学键的类型相同的是 ( )
| A.CaCl2 MgCl2 Na2O | B.H2O Na2O? CO2 |
| C.CaCl2 ? NaOH H2SO4 | D.NH4Cl H2O CO2 |