题目内容
4.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是( )| A. | H2O2分子中只存在极性键 | B. | NH3的结构式为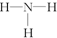 | ||
| C. | HCl的电子式为 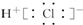 | D. | H2O中含有离子键 |
分析 A.H2O2分子中存在H-O,O-O键;
B.氨气是氮原子和氢原子之间通过共价单键形成的三角锥形结构;
C.HCl为共价化合物,电子式中不存在离子;
D.水为共价化合物.
解答 解:A.H2O2分子中存在H-O极性键,O-O非极性键,故A错误;
B.氨气是氮原子和氢原子之间通过共价单键形成的三角锥形结构,结构式为: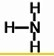 ,故B正确;
,故B正确;
C.HCl为共价化合物,电子式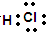 ,故C错误;
,故C错误;
D.水为共价化合物,不含离子键,故D错误;
故选:B.
点评 本题考查学生结构式的书写知识,明确物质的构成是解题关键,题目难度不大.

练习册系列答案
相关题目
9.下列各组离子能在溶液中大量共存的是( )
| A. | Mg2+、OH-、NO3-、K+ | B. | H+、HCO3-、Ca2+、NO3- | ||
| C. | Cl-、OH-、H+、K+ | D. | Cu2+、SO42-、Na+、Cl- |
10.下列叙述及解释正确的是( )
| A. | 2NO2(g)(红棕色)???N2O4(g)(无色)△H<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 | |
| B. | H2(g)+I2(g)???2HI(g)△H<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 | |
| C. | FeCl3+3KSCN???Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl,因为平衡向逆反应方向移动,故体系颜色变浅 | |
| D. | 对于N2+3H2???2NH3,平衡后,压强不变,充入O2,平衡左移 |
7.下列物质间的转化可由一步反应完成的是( )
| A. | SiO2→H2SiO3 | B. | Cu(OH)2→Fe(OH)3 | C. | CaCO3→Na2CO3 | D. | K2O→KOH |
14.下列属于苯的同系物的是( )
| A. | 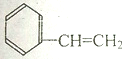 | B. | 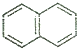 | C. |  | D. | 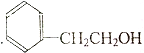 |
9.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 25℃时,pH=3的1.0L NaHSO3溶液中,含Na+数目为0.001NA | |
| B. | 常温下,1L pH=12的Ba(OH)2 溶液中含OH-的数目为2NA | |
| C. | 1L0.1mol•L-1的氨水中含有的NH3分子数小于0.1 NA | |
| D. | 在高温高压下,28gN2和6g H2充分反应生成NH3的分子数为2NA |
16.VL MgCl2溶液中,含Mg2+为mg,则该溶液中Cl-的物质的量浓度为( )
| A. | $\frac{m}{V}$mol•L-1 | B. | $\frac{m}{24V}$mol•L-1 | C. | $\frac{m}{12V}$mol•L-1 | D. | $\frac{m}{48V}$mol•L-1 |
13.含NaOH 0.5mol的稀溶液与足量稀盐酸反应,放出28.7kJ的热量,表示该反应的热化学方程式正确的是( )
| A. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+28.7 kJ•mol-1 | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-28.7 kJ•mol-1 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=+57.4 kJ•mol-1 | |
| D. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.4 kJ•mol-1 |