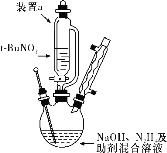
题目内容
【题目】将0.2 mol·L-1的KOH溶液与0.1 mol·L-1的H2SO3溶液等体积混合后,溶液中各粒子浓度大小关系正确的是( )
A.c(K+)+c(H+)=c(OH-)+c(![]() )+c(
)+c(![]() )
)
B.2c(K+)=c(![]() )+c(
)+c(![]() )+c(H2SO3)
)+c(H2SO3)
C.c(K+)>c(![]() )>c(
)>c(![]() )>c(H2SO3)
)>c(H2SO3)
D.c(![]() )+c(
)+c(![]() )+c(H2SO3)=0.1 mol·L-1
)+c(H2SO3)=0.1 mol·L-1
【答案】C
【解析】
根据题中溶液中各粒子浓度大小可知,本题考查溶液中离子浓度大小的比较,运用溶液中遵循电荷守恒、物料守恒及多元弱酸根阴离子分步水解分析。
等体积混合之后,发生了反应:2KOH+H2SO3=K2SO3+2H2O因为氢氧化钾浓度是亚硫酸的二倍,则两者恰好反应,生成亚硫酸钾,
A.生成的亚硫酸钾溶液中电荷守恒,阳离子所带正电荷总数等于阴离子所带负电荷总数, 则c(K+)+c(H+)=c(OH-)+c(![]() )+2c(
)+2c(![]() ),A项错误;
),A项错误;
B.生成的亚硫酸钾溶液中物料守恒, 则c(K+)=2c(![]() )+2c(
)+2c(![]() )+2c(H2SO3),B项错误;
)+2c(H2SO3),B项错误;
C.生成的亚硫酸钾溶液中因为亚硫酸根的水解作用,所以c(K+)>c(SO32-),而因为是两步水解,程度逐渐降低,而且水解程度非常微弱.所以c SO32-)>c(HSO3-)>c(H2SO3),C项正确;
D. 生成的亚硫酸钾溶液中存在物料守恒,即硫元素总物质的量是不变的;.但因为混合之后体积变为原来的二倍,则浓度应该是原来的一半,所以浓度和应该是0.05mol/L,D项错误;
答案选C。

【题目】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为__,该电子层具有的原子轨道数为__。
②LiBH4由Li+和BH4-构成,BH4-的立体构型是__,B原子的杂化轨道类型是___。
③Li、B元素的电负性由小到大的顺序为___。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+__H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是__族元素。
(3)图2是立方氮化硼晶胞沿z轴的投影图,请在图中圆球上涂“●”和涂“![]() ”分别标明B与N的相对位置___。
”分别标明B与N的相对位置___。
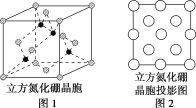
(4)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm,Na+半径为102pm,H-的半径为__,NaH的理论密度是__g·cm-3(保留3个有效数字)。
【题目】(环境污染与资源短缺问题日益突出,资源的循环利用尤为重要。工业 上利用含 Cu2O(含少量 Al2O3、Fe2O3 和 SiO2)的矿渣提取铜的工艺流程如下:

已知:①Cu2O 在酸性条件下易转化成单质 Cu 和含 Cu2+的溶液;
②几种氢氧化物沉淀时的 pH 如下表:
氢氧化物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 |
沉淀时的 pH | 4.0~5.2 | 5.8~8.8 | 1.1~3.2 | 5.4~6.7 |
回答下列问题:
(1)经检测固体 A 含有的成分为 Cu 和另一种杂质,从固体 A 中分离出 Cu 的可 用试剂为_____溶液(填化学式)。
(2)矿渣经酸浸、过滤、洗涤后铁元素的主要存在形式为__________填离子符号),检验该离子的常用化学试剂是_________________。
(3)加 NaClO 氧化并调整溶液的 pH 为_____,得到沉淀 B 和一种具有漂白 性的物质 D,该反应离子方程式为_________。
(4)25℃时,加 NaOH 固体调节溶液 pH 得到 Al(OH)3 沉淀,若 pH=5.3 时,所得 溶液中 c(Al3+)=_____。已知 25℃时 Ksp[Al(OH)3]=1.3×10-33。
(5)用惰性电极电解获得金属铜时,起始阶段阳极产物与阴极产物的物质的量之比为___________。