题目内容
3.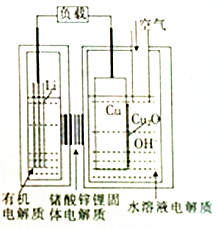 近年来AIST报告正在研究一种“高容量、低成本”锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )
近年来AIST报告正在研究一种“高容量、低成本”锂-铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,Li+透过固体电解质向Cu极移动 | |
| B. | 放电时,负极的电极反应式为Cu2O+H2O+2e-=Cu+2OH- | |
| C. | 通空气时,铜被腐蚀,表面产生Cu2O | |
| D. | 整个反应过程中,铜相当于催化剂 |
分析 放电时,锂失电子作负极,Cu上O2得电子作正极,负极上电极反应式为Li-e-═Li+,正极上电极反应式为O2+4e-+2H2O=4OH-,电解质溶液中阳离子向正极移动,阴离子向负极移动,据此分析解答.
解答 解:A.放电时,阳离子向正极移动,则Li+透过固体电解质向Cu极移动,故A正确;
B.放电时,负极的电极反应式为Li-e-═Li+,故B错误;
C.放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,可知通空气时,铜被腐蚀,表面产生Cu2O,故C正确;
D.通空气时,铜被腐蚀,表面产生Cu2O,放电时Cu2O转化为Cu,则整个反应过程中,铜相当于催化剂,故D正确;
故选B.
点评 本题考查了原电池原理,明确原电池负极上得失电子及电极反应式是解本题关键,题目难度中等,注意把握Cu在整个过程中的作用.

练习册系列答案
相关题目
8.下列物质中含有非极性键的共价化合物是( )
| A. | CCl4 | B. | Na2O2 | C. | C2H4 | D. | CS2 |
15.为了实现绿色化学,符合工业生产实际的是( )
| A. | 用纯碱吸收硫酸工业的尾气 | B. | 用烧碱吸收氯碱工业的尾气 | ||
| C. | 用纯碱吸收合成氨工业的尾气 | D. | 用烧碱吸收炼铁工业的尾气 |
13. 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )| A. | 该混合气体中一定含有乙烯 | |
| B. | 该混合气体中有且只有一种烷烃 | |
| C. | 组成该混合气体的烃分子所含氢原子数均为4 | |
| D. | 若混合气体由CH4和C2H4组成,则其体积比为2:3 |
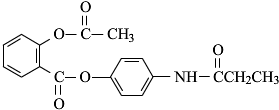 ,由它可衍生出一系列物质,有关变化如图:
,由它可衍生出一系列物质,有关变化如图: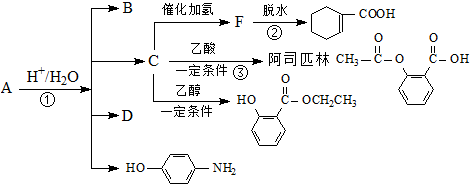
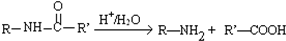
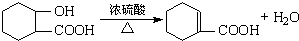 .
.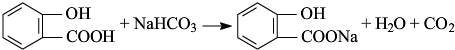 .
.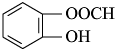 (或间位或对位).
(或间位或对位).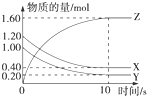 (1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则
(1)某温度下,2L恒容密闭容器中,X、Y、Z三种气体发生化学反应时,物质的量随时间变化的关系曲线如图所示,则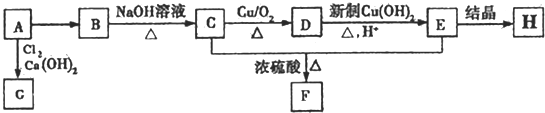
 .
.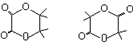 .
.