题目内容
【题目】向物质的量各有1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2溶液,产生沉淀的量随着Ba(OH)2 加入量的变化如图所示。下列离子方程式书写正确的是
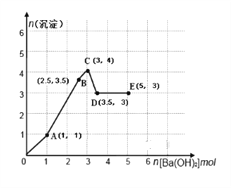
A. O→A:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B. A→B:2Al3++3SO42-+3Ba2+ +6OH-=3BaSO4↓+2Al(OH)3↓
C. B→C:NH4++SO42-+Ba2+ +OH-=BaSO4↓+NH3·H2O
D. D→E:NH4++ OH-=NH3·H2O
【答案】B
【解析】试题分析:1mol的NH4Al(SO4)2和H2SO4混合稀溶液中逐滴加入一定量Ba(OH)2 溶液,A(1,1)可知,发生硫酸和氢氧化钡的离子反应;A→B发生硫酸根离子、铝离子与氢氧化钡的离子反应生成两种沉淀;B→C发生铵根离子、硫酸根离子与氢氧化钡飞离子反应;C→D发生氢氧化铝的溶解离子反应;D→E没有离子反应发生,则A、O→A的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,A错误;B、A→B的离子反应为2Al3++3SO42ˉ+3Ba2++6OHˉ=3BaSO4↓+2Al(OH)3↓,B正确;C、B→C的离子反应为2NH4++SO42ˉ+Ba2++2OHˉ=BaSO4↓+2NH3·H2O,C错误;D、D→E没有离子反应发生,不能写出离子反应,D错误,答案选B。

练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目