题目内容
在醋酸中存在电离平衡:CH3COOH  CH3COO-+H+,要使溶液中的c(CH3COO-)提高,应采取的措施是( )
CH3COO-+H+,要使溶液中的c(CH3COO-)提高,应采取的措施是( )
 CH3COO-+H+,要使溶液中的c(CH3COO-)提高,应采取的措施是( )
CH3COO-+H+,要使溶液中的c(CH3COO-)提高,应采取的措施是( )| A.加水 | B.加热 | C.加CH3COONa固体 | D.加很稀的NaOH溶液 |
BC
试题分析:在醋酸中存在电离平衡:CH3COOH
 CH3COO-+H+,要使溶液中的c(CH3COO-)提高,可以加入可以提供CH3COO-的盐,故选C,加热可以使平衡向吸热方向移动,故选B,加水会稀释使浓度降低;加很稀的NaOH溶液,同样相当于稀释;故选BC。
CH3COO-+H+,要使溶液中的c(CH3COO-)提高,可以加入可以提供CH3COO-的盐,故选C,加热可以使平衡向吸热方向移动,故选B,加水会稀释使浓度降低;加很稀的NaOH溶液,同样相当于稀释;故选BC。点评:以下列表归纳了外界条件变化对电离平衡及c(H+)的影响,这里假设弱电解质AB可以电离成(A+)和(B-),且电离过程吸热,
则
| 电离方程式 | AB=(可逆反应)=(A+)+(B-) | |
| 条件改变内容 | v(正),v(逆)关系 | 平衡移动方向 |
| 增大c(AB) | v(正)>v(逆) | 向右 |
| 减小c(AB) | v(正)<v(逆) | 向左 |
| 增大c(A+) | v(正)<v(逆) | 向左 |
| 减小c(A+) | v(正)>v(逆) | 向右 |
| 增大c(B—) | v(正)<v(逆) | 向左 |
| 减小c(B—) | v(正)>v(逆) | 向右 |
| 稀释溶液 | v(正)>v(逆) | 向右 |
| 升高温度 | v(正)>v(逆) | 向右 |
| 降低温度 | v(正)<v(逆) | 向左 |

练习册系列答案
相关题目
 2C(g) △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是
2C(g) △H<0。t1时刻达到平衡后,在t2时刻改变某一条件,其反应过程如图。下列说法正确的是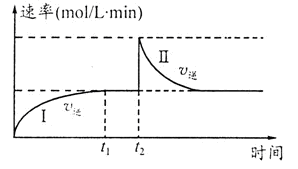
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示: CO(g)+H2O(g)
CO(g)+H2O(g)

 CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1
CH3OH(g) +H2O(g) △H=-49.0 kJ·mol-1 
 2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
 4HCl+Si
4HCl+Si Z(g);△H <0
Z(g);△H <0 
 xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
xC(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下: