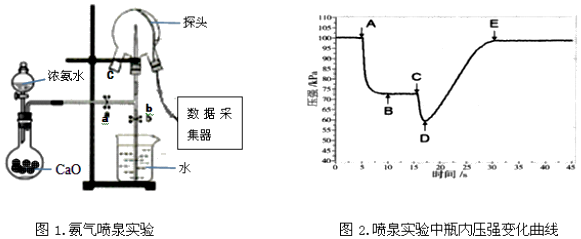
��Ŀ����
����Ŀ���״��ȿ����ڻ����л�ԭ�ϣ��ֿ���Ϊȼ�������������ȼ�ϣ�
��1�������ǹ�ҵ�Ϻϳɼ״��ķ�Ӧ��CO��g��+2H2��g��CH3OH��g����H �±����������Ǹ÷�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶� | 250�� | 300�� | 350�� |
K | 2.041 | 0.270 | 0.012 |
�ɱ��������жϷ�ӦIΪ�ȷ�Ӧ��������š�����
ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c��CO��=0.2mol/L����CO��ת����Ϊ �� ��ʱ���¶�Ϊ���ӱ���ѡ��
��2����֪�ڳ��³�ѹ�£� ��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1 kJ/mol
��2CO��g��+O2��g��=2CO2��g����H2 kJ/mol
��H2O��g��=H2O��l����H3 kJ/mol
��Ӧ CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=kJ/mol���á�H1����H2����H3��ʾ��
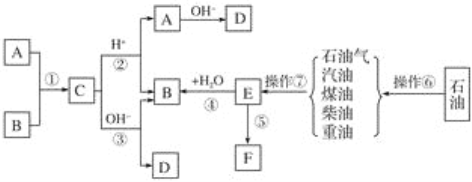
��3�����Լ״�ȼ�ϵ�أ����õ�ⷨ���������Ժ�����ˮ����Ҫ����Cr2O72��ʱ��ʵ����������ͼװ��ģ��÷��� 
��N�缫�ĵ缫��ӦʽΪ ��
������ɵ�����Cr2O72ת��ΪCr3+�����ӷ�Ӧ����ʽ��
Cr2O72+Fe2++�TCr3++Fe3++
��4��������ˮʱ�����Cr3+��Cr��OH��3��ʽ��ȥ����c��Cr3+��=1��10-5molL��1 ʱ��Cr3+������ȫ����ʱ��Һ��pH= �� ����֪��Ksp=6.4��10-31 �� lg2=0.3��
���𰸡�
��1���ţ�80%��250��
��2������H1����H2+4��H3��/2
��3��O2+4e��+4H+=2H2O��6��14H+��2��6��7H2O
��4��5.6
���������⣺��1���ɱ������ݿ�֪�����¶�����ƽ�ⳣ����С��˵�������¶�ƽ�������ƶ���������ӦΪ���ȷ�Ӧ���ʡ�H��0��ij�¶��£���2molCO��6molH2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c��CO��=0.2mol/L����
CO��g��+ | 2H2��g���T | CH3OH��g�� | |
��ʼ��mol�� | 1 | 3 | 0 |
ת����mol�� | 0.8 | 1.6 | 0.8 |
ƽ�⣨mol�� | 0.2 | 1.4 | 0.8 |
COת����= ![]() ��100%=80%��ƽ�ⳣ��K=
��100%=80%��ƽ�ⳣ��K= ![]() =
= ![]() =2.041�����¶�Ϊ250�棬
=2.041�����¶�Ϊ250�棬
���Դ��ǣ��ţ�80%��250�棻��2����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1 kJ/mol
��2CO��g��+O2��g��=2CO2��g����H2 kJ/mol
��H2O��g��=H2O��l����H3 kJ/mol
���ݸ�˹���� ![]() ���٩���+4�ۣ��ɵã�CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=����H1����H2+4��H3��/2kJ/mol��
���٩���+4�ۣ��ɵã�CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=����H1����H2+4��H3��/2kJ/mol��
���Դ��ǣ�����H1����H2+4��H3��/2����3���������������ӽ���Ĥ��M�缫������N�缫������MΪ������NΪ�����������Ϸ���������Ӧ���״�ʧȥ���ӣ����ɶ�����̼�������ӣ������缫��ӦʽΪ��CH3OH��6e��+H2O=6H++CO2��������������ԭ��Ӧ��������õ��ӣ���ͨ�����ӽ���Ĥ�������ӽ��Ϊˮ�������缫��ӦʽΪ��O2+4e+4H+=2H2O��
���Դ��ǣ�O2+4e+4H+=2H2O��
�ڵ�����Һ��Cr2O72��ת��ΪCr3+�����ϼ۽���6�ۣ����Fe�缫Ϊ������Feʧȥ��������Fe2+����������Fe2+��Cr2O72����ԭΪCr3+������������ΪFe3+�����ϼ����߹�1�ۣ����ϼ�������С������Ϊ6����Cr2O72����ϵ��Ϊ1��Fe2+��ϵ��Ϊ6����Ӧ���ӷ���ʽΪ��Cr2O72��+6Fe2++14H+=2Cr3++6Fe3++7H2O��
���Դ��ǣ�1��6��14H+��2��6��7H2O����4��Ksp=c��Cr3+����c3��OH����=6.4��1031��c��Cr3+��=1��105molL��1 ʱ����Һ��c��OH����=4��109molL��1����c��H+��= ![]() mol/L=2.5��106molL��1����pH=��lg2.5��106=5.6��
mol/L=2.5��106molL��1����pH=��lg2.5��106=5.6��
���Դ��ǣ�5.6��
�����㾫����ͨ��������÷�Ӧ�Ⱥ��ʱ䣬�����ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȼ����Խ����⣮

����Ŀ��ijͬѧ��SO2��Cl2�Ļ�������м���Ʒ����Һ������Һ��ɫ��������ɫ��Һ�ֳ����ݣ����ν���ʵ�飬ʵ�������ʵ�������¼���£�
��� | |||
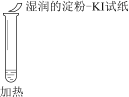
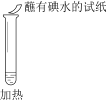
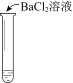
ʵ����� |
|
|
|
ʵ������ | ��Һ����죬��ֽ������ | ��Һ����죬��ֽ��ɫ | ���ɰ�ɫ���� |
����ʵ������У�����ȷ����
A. ��˵��Cl2����ȫ����
B. ������ֽ��ɫ��ԭ���ǣ�SO2 + I2 + 2H2O == H2SO4 + 2HI
C. ��������BaCl2��Һ����Ba(NO3)2��Һ��Ҳ��˵��SO2��Cl2����ΪSO42
D. ʵ�������£�Ʒ����Һ��SO2��������