题目内容
下列关于金属铝的叙述中,说法正确的是
| A.Al是地壳中含量最多的元素 |
| B.Al是比较活泼的金属,在化学反应中容易失去电子,表现氧化性 |
| C.与Al反应产生H2的溶液一定呈酸性 |
| D.Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al并不滴落 |
D
试题分析:A、Al 是地壳中含量最多的金属元素但不是元素,最多的是氧元素,故错误;B.Al是比较活泼的金属,在化学反应中容易失去电子,表现还原性,错误。C、与Al反应产生H2的溶液并不一定呈酸性,如强碱溶液,故错;D、铝的熔点较高,受热不易溶化;Al在常温下与空气里的氧气反应,生成一层致密而坚固的氧化物薄膜,熔化的Al并不滴落,故对。故选D

练习册系列答案
相关题目
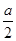 mol/L。
mol/L。
 Al2(SO4)3+
Al2(SO4)3+