题目内容
【题目】在配制一定物质的量浓度的NaOH溶液时,下列哪个原因会造成所配溶液浓度偏高( )B
A. 所用NaOH已经潮解 B. 向容量瓶中加水未到刻度线
C. 有少量NaOH溶液残留在烧杯里 D. 称量时误用“左码右物”且使用了游码
【答案】B
【解析】试题分析:根据c=m/MV=n/V,A、氢氧化钠潮解,溶质的质量减小,所配物质的量浓度偏低,故错误;B、未加水到刻度线,溶液体积减小,物质的量浓度偏高,故正确;C、少量氢氧化钠溶液残留在烧杯中,溶质的质量减小,浓度偏低,故错误;D、造成溶质的质量减小,物质的量浓度偏低,故错误。

练习册系列答案
相关题目
【题目】实验室中某些气体的制取、收集、尾气处理(或性质实验)装置如图所示,用此装置和下表中提供的物质完成相关实验,其中合理的选项是
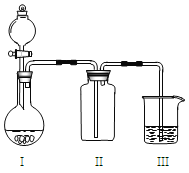
选项 | I中的物质 | II中收集的气体 | III中的物质 |
A | Cu和浓硝酸 | NO | NaOH溶液 |
B | 浓盐酸和高锰酸钾 | Cl2 | NaOH溶液 |
C | 大理石和稀硫酸 | CO2 | 澄清石灰水 |
D | 浓氨水和CaO | NH3 | 滴加酚酞的水 |
A. A B. B C. C D. D
