题目内容
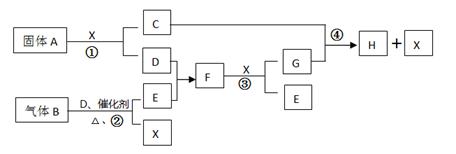
(8分)A、B、C、D、E、F、G、H、I、J、K都是中学课本常见物质,它们与X具有下图相互转化关系。

已知:①A、D、E、K为单质,其中E为黑色固体;
②X、A、B、C、D为气体,B、C均能使澄清石灰水变浑浊,C、D均能使品红溶液褪色;
③H是一种红棕色固体氧化物。
请回答下列问题:
(1)B分子的电子式:_______________;
(2)J与氨水反应的离子方程式:_______________________________________;
反应全过程的现象是:_____________________________________________;
(3)E和F反应的化学方程式:__________________________________________;
(4)气体X中含有三种元素,分子中各原子均达到8电子稳定结构,其对H2的相对密度为30,试推断X的分子式:___________;X的结构式:____________。

已知:①A、D、E、K为单质,其中E为黑色固体;
②X、A、B、C、D为气体,B、C均能使澄清石灰水变浑浊,C、D均能使品红溶液褪色;
③H是一种红棕色固体氧化物。
请回答下列问题:
(1)B分子的电子式:_______________;
(2)J与氨水反应的离子方程式:_______________________________________;
反应全过程的现象是:_____________________________________________;
(3)E和F反应的化学方程式:__________________________________________;
(4)气体X中含有三种元素,分子中各原子均达到8电子稳定结构,其对H2的相对密度为30,试推断X的分子式:___________;X的结构式:____________。
(1)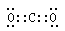
(2)Fe2++2NH3·H2O= Fe(OH)2↓+2NH4+
先生成白色沉淀,立即变为灰绿色,最终呈红褐色
(3)C+2H2SO4(浓)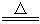 CO2↑+2 SO2↑+ 2H2O
CO2↑+2 SO2↑+ 2H2O
(4)SCO S=C=O
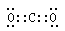
(2)Fe2++2NH3·H2O= Fe(OH)2↓+2NH4+
先生成白色沉淀,立即变为灰绿色,最终呈红褐色
(3)C+2H2SO4(浓)
 CO2↑+2 SO2↑+ 2H2O
CO2↑+2 SO2↑+ 2H2O(4)SCO S=C=O
B、C均为气体且均能使澄清石灰水变浑浊,C能使品红溶液褪色,综合可判定B为CO2,C为SO2;而A为气体单质,与X气体燃烧可生成CO2与SO2,可知A为氧气,且X物质中含有最起码含有碳、硫元素;
C(SO2)、D均能使品红溶液褪色,且均为气体,猜测D为氯气(或臭氧等):Cl2+SO2+2H2O=H2SO4+2HCl;而黑色固体单质E可与A(氧气)燃烧生成CO2,则E为碳,碳与F可生成CO2、SO2及水,则可判定F为硫酸,而G为盐酸;
H是一种红棕色固体氧化物,也就是Fe2O3,与盐酸反应生成I,即FeCl3:Fe2O3+6HCl=2FeCl3+3H2O;J物质可与D(氯气)生成FeCl3,可知J为FeCl2,K为铁单质
(1)CO2为直线型分子,两个碳氧双键: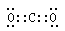
(2)制取 Fe(OH)2:Fe2++2NH3·H2O= Fe(OH)2↓+2NH4+
Fe(OH)2易被氧化,先生成白色沉淀,立即变为灰绿色,最终呈红褐色 Fe(OH)3
(3)C+2H2SO4(浓) CO2↑+2 SO2↑+ 2H2O
CO2↑+2 SO2↑+ 2H2O
(4)由题意知,分子中一定含有S和C原子,并且燃烧生成SO2与CO2,故第三种元素只能为O元素;相对分子质量为30×2=60,说明分子式只能为SCO;
分子中各原子均达到8电子稳定结构,则C形成四键,O、S均为二键,联系CO2的结构可得X的结构式为:S=C=O
C(SO2)、D均能使品红溶液褪色,且均为气体,猜测D为氯气(或臭氧等):Cl2+SO2+2H2O=H2SO4+2HCl;而黑色固体单质E可与A(氧气)燃烧生成CO2,则E为碳,碳与F可生成CO2、SO2及水,则可判定F为硫酸,而G为盐酸;
H是一种红棕色固体氧化物,也就是Fe2O3,与盐酸反应生成I,即FeCl3:Fe2O3+6HCl=2FeCl3+3H2O;J物质可与D(氯气)生成FeCl3,可知J为FeCl2,K为铁单质
(1)CO2为直线型分子,两个碳氧双键:
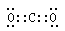
(2)制取 Fe(OH)2:Fe2++2NH3·H2O= Fe(OH)2↓+2NH4+
Fe(OH)2易被氧化,先生成白色沉淀,立即变为灰绿色,最终呈红褐色 Fe(OH)3
(3)C+2H2SO4(浓)
 CO2↑+2 SO2↑+ 2H2O
CO2↑+2 SO2↑+ 2H2O(4)由题意知,分子中一定含有S和C原子,并且燃烧生成SO2与CO2,故第三种元素只能为O元素;相对分子质量为30×2=60,说明分子式只能为SCO;
分子中各原子均达到8电子稳定结构,则C形成四键,O、S均为二键,联系CO2的结构可得X的结构式为:S=C=O

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
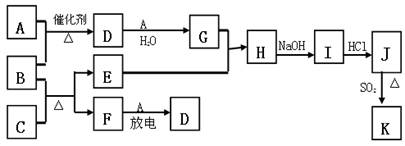
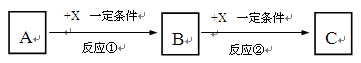

 ,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。
,X的阳离子与Y的阴离子的电子层结构相同。元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子。 ]2-
]2- 
