题目内容
【题目】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知E(N-N)=a kJ/mol,E(N≡N)=b kJ/mol,E(N-H)=c kJ/mol,E(H-O)=d kJ/mol,E(O=O)=e kJ/mol,则:
N2H4(g)+O2(g)=N2(g)+2H2O(l) △H=____________________kJ·mol-1
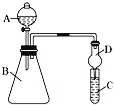
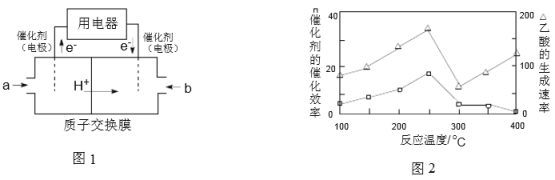
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图1所示,则通入a气体的电极名称为 ,通入b气体的电极反应式为 。(质子交换膜只允许H+通过)
(3)在一定温度和催化剂作用下,CH4和CO2可直接生成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图2所示,则该反应的最佳温度控制在 左右。
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2,难容物),将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 。
(4)CH4还原法是处理NOX气体的一种方法。已知一定条件下CH4与NOX反应转化为N2和CO2,若标准状况下8.96L CH4可处理22.4L NOX,则X值为 。
【答案】
(1)(a+4c+e-b-4d);
(2)负极;O2+4e-+4H+=2H2O;
(3)①250℃;②3CuAlO2+16H++NO3-=NO↑+3Al3++3Cu2++8H2O;
(4)1.6。
【解析】
试题分析:(1)反应热就是断裂反应物化学键吸收的能量与形成生成物的化学键释放的能量差,则E(N-N)=a kJ/mol,E(N≡N)=b kJ/mol,E(N-H)=c kJ/mol,E(H-O)=d kJ/mol,E(O=O)=e kJ/mol,所以N2H4(g)+O2(g) =N2(g)+2H2O(l) △H=(a+4c+e-b-4d) kJ/mol;(2)由图可知,通入气体a的一端失去电子发生氧化反应,故a电极应通入甲烷,该极为负极,通入b的气体为氧气,获得电子,酸性条件下生成水,是正极;正极电极反应式为:O2+4e-+4H+=2H2O;(3)①250℃时乙酸反应速率最大、催化活性,故选择250℃;②CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,生成的盐为硝酸铝、硝酸铜,反应还有水生成,反应离子方程式为:3CuAlO2+16H++NO3-=NO↑+3Al3++3Cu2++8H2O;(4)根据氧化还原反应中电子转移守恒,可得:8.96L×[4-(-4)]=22.4L×2x,解得x=1.6。

【题目】I如表所示为元素周期表的一部分,参照元素①~⑩在表中的位置,请回答下列问题:
族 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(1)写出①和④两种元素原子按1:1组成的常见化合物的电子式 。
(2)用电子式表示⑥和⑨形成化合物的过程: 。
(3)③、⑧、⑩的最高价氧化物对应水化物的酸性由强到弱的顺序为 (用化学式表示)。
(4)已知周期表中存在对角相似规则,如②与⑦在周期表中处于对角线位置则化学性质相似,②的氧化物、氢氧化物也有两性,写出②的氢氧化物与⑥的氢氧化物反应的化学方程式 。
(5)⑤、⑥、⑩的离子半径由大到小的顺序为 (用离子符号表示)。
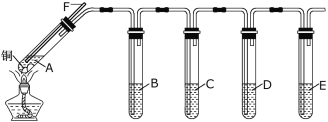
II某同学欲利用下图装置验证同主族元素性质递变规律。若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4,(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C溶液中现象为 ,反应离子方程式为 ,即可证明。