题目内容
12.某小分子抗癌药物的分子结构如图所示,下列说法正确的是( )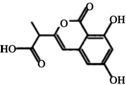
| A. | 1mol该有机物最多可以和4mol Na反应 | |
| B. | 该有机物容易发生加成、取代、中和、消去等反应 | |
| C. | 该有机物遇FeCl3溶液不变色,但可使酸性KMnO4溶液褪色 | |
| D. | 1mol该有机物与浓溴水反应,最多消耗3mol Br2 |
分析 由图可知,分子中含酚-OH、-COOH、-COOC-、碳碳双键,结合酚、羧酸、酯、烯烃的性质来解答.
解答 解:A.只有酚-OH、-COOH与Na反应,则1mol该有机物最多可以和3mol Na反应,故A错误;
B.该有机物容易发生加成、取代、中和反应,不能发生消去反应,故B错误;
C.含酚-OH,遇FeCl3溶液变色,可使酸性KMnO4褪色,故C错误;
D.酚-OH的邻对位与溴水反应,碳碳双键与溴水发生加成反应,1mol该有机物与浓溴水反应,最多消耗3mol Br2,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸、酯、烯烃的性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列各组内的两种物质互为同素异形体的是( )
| A. | 16O和18O | B. | O2和O3 | C. | 乙烷和丙烷 | D. | 乙酸和甲酸甲酯 |
3.如图是研究氯气性质的装置图,其中气体M的主要成分是氯气,杂质是氯化氢和水蒸气.回答下列问题: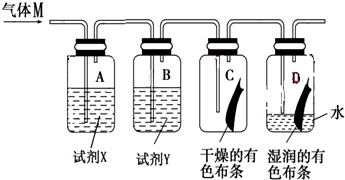
(1)装置A、B中的试剂X和试剂Y分别是b(填字母代号).
a.NaOH溶液 浓硫酸 b.NaCl溶液 浓硫酸 c.浓硫酸 石灰水
(2)若C中有色布条不褪色,D中有色布条褪色.则具有漂白性的物质是次氯酸(填物质名称),该实验证明氯气能与水反应,反应的离子方程式为Cl+H2O=H++Cl-+HClO.
(3)从绿色化学的角度分析,上述实验装置图中存在一处缺陷,改正的方法是加一个尾气处理装置,该尾气处理装置内发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(4)实验完毕后,将D中的水溶液(呈黄绿色)取出,分别加入两支试管中,进行如下实验

(1)装置A、B中的试剂X和试剂Y分别是b(填字母代号).
a.NaOH溶液 浓硫酸 b.NaCl溶液 浓硫酸 c.浓硫酸 石灰水
(2)若C中有色布条不褪色,D中有色布条褪色.则具有漂白性的物质是次氯酸(填物质名称),该实验证明氯气能与水反应,反应的离子方程式为Cl+H2O=H++Cl-+HClO.
(3)从绿色化学的角度分析,上述实验装置图中存在一处缺陷,改正的方法是加一个尾气处理装置,该尾气处理装置内发生反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O.
(4)实验完毕后,将D中的水溶液(呈黄绿色)取出,分别加入两支试管中,进行如下实验
| 实验编号 | 滴加的试剂 | 实验现象 | 证明存在的微粒 (填微粒符号) |
| A | AgNO3 溶液 | a.产生白色沉淀 | b.Cl- |
| B | 紫色石蕊溶液 | c.先变红色后褪色 | d.H+,HClO |
17.下列物质中,不含有硅酸盐的是( )
| A. | 水玻璃 | B. | 太阳能电池 | C. | 黏土 | D. | 普通水泥 |
4.二氧化硅是酸性氧化物是因为( )
| A. | 硅是非金属 | |
| B. | 它是非金属氧化物 | |
| C. | 二氧化硅能跟氢氧化钠反应生成盐和水 | |
| D. | 它的对应水化物是弱酸,能溶于水 |
1.甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用如图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验).
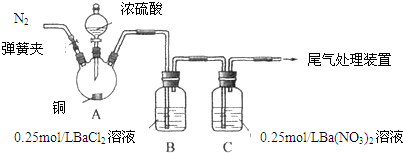
实验操作和现象:
(1)A中反应的化学方程式是Cu+2H2SO4$\stackrel{△}{→}$CuSO4+SO2↑+2H2O.
(2)C中白色沉淀是Ba2SO4,该沉淀的生成表明SO2具有还原性.
(3)C中液面上方生成浅棕色气体的化学方程式是2NO+O2=2NO2.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是通N2一段时间,排除装置中的空气;乙在A、B间增加洗气瓶D,D中盛放的试剂是饱和NaHSO3溶液.
②进行实验,B中现象:甲--有大量白色沉淀;乙--有少量白色沉淀检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原因:甲:SO42-+Ba2+→BaSO4↓,乙:2Ba2++2SO2+O2+2H2O→2BaSO4↓+4H+
白雾的量远多于装置中O2的量.
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀.

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | --- |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中白色沉淀是Ba2SO4,该沉淀的生成表明SO2具有还原性.
(3)C中液面上方生成浅棕色气体的化学方程式是2NO+O2=2NO2.
(4)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应.
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是通N2一段时间,排除装置中的空气;乙在A、B间增加洗气瓶D,D中盛放的试剂是饱和NaHSO3溶液.
②进行实验,B中现象:甲--有大量白色沉淀;乙--有少量白色沉淀检验白色沉淀,发现均不溶于稀盐酸.结合离子方程式解释实验现象异同的原因:甲:SO42-+Ba2+→BaSO4↓,乙:2Ba2++2SO2+O2+2H2O→2BaSO4↓+4H+
白雾的量远多于装置中O2的量.
(5)合并(4)中两同学的方案进行实验.B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是SO2与可溶性钡的强酸盐不能反应生成BaSO3沉淀.
2.下列各组物质中化学键的类型相同的是( )
| A. | HCl MgCl2NH4Cl | B. | H2O Na2O? CO2 | ||
| C. | CaCl2? NaOH H2O | D. | NH3•H2O CO2 |
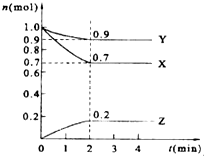 某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.