题目内容
【题目】某学习小组为研究铜与浓、稀HNO3反应的差异,设计了如图所示的实验装置。

下列说法不正确的是
A. 反应开始前通入过量的CO2气体,目的是排除装置内的空气
B. A中的离子方程式为:Cu+2NO3-+4H+==Cu2++2NO2↑+2H2O
C. 当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol
D. C装置中装入一定量的水进行尾气处理
【答案】D
【解析】研究铜与浓、稀HNO3反应的差异,先利用二氧化碳将装置中的空气排出,防止Cu与稀硝酸反应生成的NO被氧化,滴加浓硝酸时Cu与浓硝酸反应生成二氧化氮,在B中发生3NO2+H2O=2HNO3+NO、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,C中收集到NO气体,最后尾气处理,则A. 反应开始前通入过量的CO2气体,目的是排除装置内的空气,A正确;B. A中铜与浓硝酸反应的离子方程式为:Cu+2NO3-+4H+=Cu2++2NO2↑+2H2O,B正确;C. B中发生3NO2+H2O=2HNO3+NO、3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,因此当B中0.03 mol铜粉被氧化时,B中产生的NO气体大于0.02 mol,C正确;D. NO不溶于水,C装置中装入一定量的水不能进行尾气处理,D错误,答案选D。

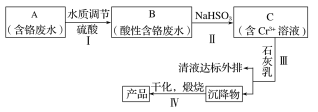
【题目】某铬盐厂净化含Cr(Ⅵ)废水并提取Cr2O3的一种工艺流程如图所示。
已知:Ksp[Cr(OH)3]=6.3×10-31
Ksp[Fe(OH)3]=2.6×10-39
Ksp[Fe(OH)2]=4.9×10-17
(1)步骤Ⅰ中,发生的反应为2H++2CrO42-![]() Cr2O72-+H2O,B中含铬元素的离子有___(填离子符号)。
Cr2O72-+H2O,B中含铬元素的离子有___(填离子符号)。
(2)当清液中Cr3+的浓度≤1.5mg·L-1时,可认为已达铬的排放标准。若测得清液的pH=5,则清液尚不符合铬的排放标准,因为此时Cr3+的浓度=__mg·L-1。
(3)步骤Ⅱ还可用其他物质代替NaHSO3作还原剂。
①若用FeSO4·7H2O作还原剂,步骤Ⅲ中参加反应的阳离子一定有__(填离子符号)。
②若用铁屑作还原剂,当铁的投放量相同时,经计算,C溶液的pH与c(Cr2O72-)的对应关系如下表所示:
pH | 3 | 4 | 5 | 6 |
c(Cr2O72-)/mol·L-1 | 7.02×10-21 | 7.02×10-7 | 1.25×10-3 | 2.21×10-34 |
有人认为pH=6时,c(Cr2O72-)变小的原因是Cr2O72-基本上都已转化为Cr3+。这种说法是否正确,为什么?___。
③用铁屑作还原剂时,为使所得产品中含铁元素杂质的含量尽可能低,需要控制的条件有___。
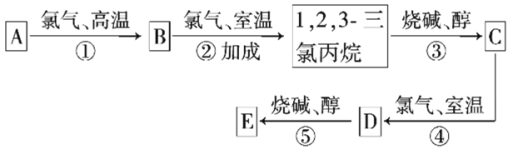
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下图所示:
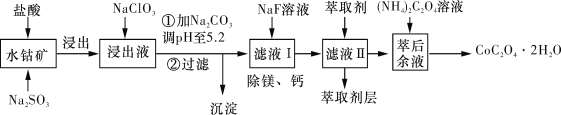
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②酸性条件下,ClO3-不会氧化Co2+,ClO3-转化为Cl-;
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)浸出过程中加入Na2SO3的主要目的是_______________________。
(2)向浸出液中加入NaClO3的离子反应方程式:_____________________。
(3)已知:常温下NH3·H2O![]() NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5
H2C2O4![]() H++HC2O4- Ka1=5.4×10-2
H++HC2O4- Ka1=5.4×10-2
HC2O4-![]() H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH____7 (填“>”或“<”或“=”)。
(4)加入(NH4)2C2O4溶液后析出晶体,再过滤、洗涤,洗涤时可选试剂_____(填字母代号)。
A.蒸馏水 B.自来水 C.饱和的(NH4)2C2O4溶液 D.稀盐酸
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,萃取剂的作用是除去锰离子,其使用的适宜pH范围是_________(填字母代号)。
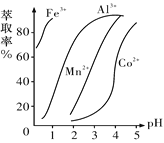
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
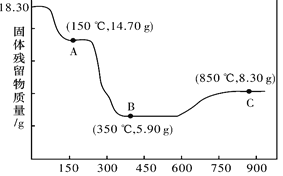
(6)CoC2O4·2H2O热分解质量变化过程如图所示。其中600℃以前是隔绝空气加热,600℃以后是在空气中加热。A、B、C均为纯净物;C点所示产物的化学式是_____________。