题目内容
1.酸与碱发生反应时,除生成正盐,如NaCl、K2SO4等外,还可能生成酸式盐,如NaHSO4、NaHCO3、NH4HCO3等,或者生成碱式盐,如碱式氯化镁[Mg(0H)Cl]、碱式碳酸铜:[Cu2(0H)2CO3]等.请回答下列问题:
(1)CO2与Na0H溶液反应,可能生成正盐--碳酸钠,也可能生成酸式盐--碳酸氢钠.你认为在什么条件下会生成碳酸氢钠CO2过量时.
(2)你认为碱式氯化镁或碱式碳酸铜等碱式盐能与盐酸发生反应吗?如果能反应,写出有关反应的化学方程式;如果不能反应.说明理由Mg(0H)Cl+HCl=H2O+MgCl2,Cu2(0H)2CO3+4HCl=2CuCl2+3H2O+CO2↑.
(3)你认为NaHSO4或NaHCO3等酸式盐能与Na0H溶液反应吗?如果能反应,写出有关反应的化学方程式;如果不能反应,说明理由NaHSO4+NaOH=H2O+Na2SO4,NaHCO3+NaOH=Na2CO3+H2O.
分析 (1)CO2与Na0H溶液反应时,在CO2不足时生成正盐,在CO2过量时生成酸式盐;
(2)碱式氯化镁[Mg(0H)Cl]和盐酸能生成水;碱式碳酸铜:[Cu2(0H)2CO3]和盐酸反应能生成水和二氧化碳;
(3)NaHSO4或NaHCO3等酸式盐中含氢离子,能和氢氧化钠反应生成水.
解答 解:(1)CO2与Na0H溶液反应时,在CO2不足时生成正盐--碳酸钠,在CO2过量时生成酸式盐--碳酸氢钠,故答案为:CO2过量时;
(2)碱式氯化镁[Mg(0H)Cl]和盐酸能生成水,符合复分解反应发生的条件,化学方程式为:Mg(0H)Cl+HCl=H2O+MgCl2;碱式碳酸铜:[Cu2(0H)2CO3]和盐酸反应能生成水和二氧化碳,也符合复分解反应发生的条件,化学方程式为:Cu2(0H)2CO3+4HCl=2CuCl2+3H2O+CO2↑,故答案为:Mg(0H)Cl+HCl=H2O+MgCl2;Cu2(0H)2CO3+4HCl=2CuCl2+3H2O+CO2↑;
(3)NaHSO4或NaHCO3等酸式盐中含氢离子,均能和氢氧化钠反应生成水,故均能和NaOH反应:NaHSO4+NaOH=H2O+Na2SO4,NaHCO3+NaOH=Na2CO3+H2O,故答案为:NaHSO4+NaOH=H2O+Na2SO4,NaHCO3+NaOH=Na2CO3+H2O;
点评 本题考查了复分解反应发生的条件以及复分解反应的书写,复分解反应发生的条件是有沉淀、气体或弱电解质生成,难度不大,注意基础的掌握.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
11.只用水就能鉴别的一组物质是( )
| A. | 乙醛、乙二酸、硝基苯 | B. | 乙醇、乙醛、乙酸 | ||
| C. | 苯、乙酸、四氯化碳 | D. | 苯酚、乙醇、甘油 |
12.某质量分数为10%的NaOH溶液,加热蒸发掉100g水后,得到的溶质质量分数为20%的NaOH溶液80mL,这80mL溶液中溶质的物质的量浓度为( )
| A. | 6.25mol/L | B. | 7mol/L | C. | 7.5mol/L | D. | 12.5mol/L |
16.某无色透明溶液中可能存在的离子组是( )
| A. | Mg2+、Ba2+、Cu2+、Cl- | B. | Fe3+、Fe2+、SO${\;}_{4}^{2-}$、NO${\;}_{3}^{-}$ | ||
| C. | H+、Mg2+、MnO${\;}_{4}^{-}$、NO${\;}_{3}^{-}$ | D. | Na+、K+、NO${\;}_{3}^{-}$、Cl- |
13.下列反应的离子方程式中,正确的是( )
| A. | KCl溶液与Na2CO3溶液反应:2K++CO32-═K2CO3 | |
| B. | 氧化镁与盐酸反应:MgO+2H+═Mg2++H2O | |
| C. | 碳酸氢钠与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 碳酸钠与氯化钙反应:Na2CO3+Ca2+═CaCO3↓+2Na+ |
10.下列反应转化关系(未配平)肯定不正确的是( )
| A. | Cu2O+H2SO4→CuSO4+Cu+H2O | B. | FeO+HNO3→Fe(NO3)3+H2O | ||
| C. | NH4NO3→N2+H2O | D. | S+KOH→K2SO3+K2S+H2O |
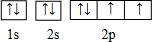 ,其电子的自旋方向共有2种.比较两种同主族非金属元素形成的单质的氧化性(用化学方程式表示)2H2S+O2=2S↓+2H2O
,其电子的自旋方向共有2种.比较两种同主族非金属元素形成的单质的氧化性(用化学方程式表示)2H2S+O2=2S↓+2H2O