��Ŀ����
����Ŀ�������£�ij�ݻ��̶����ܱ������ɿ��ƶ��Ļ�������A��B���ң��ֱ���A��B���ҳ���H2��O2�Ļ�������1 mol��������ʱ������λ����ͼ��ʾ��
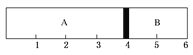
��1��A�һ����������ʵ���Ϊ________��������������Ϊ________��
��2��ʵ����A�һ�����������Ϊ34 g����û��������ܶ���ͬ��ͬѹ�����º����ܶȵ�________����
��3������A��H2��O2�Ļ�������ȼ�������ָ�ԭ�¶Ⱥ����ջ���ͣ����λ����________�̶ȣ�����������ѹǿ�뷴Ӧǰ����ѹǿ֮��Ϊ________��
���𰸡� 2 mol 2NA(��1.204��1024) 4.25 2 1��2
�������������������1��ͬ��ͬѹ�£����֮�ȵ������ʵ���֮�ȣ�4/2=n(�������)/1����˻����������ʵ���Ϊ2mol��������������Ϊ2NA����2��ͬ��ͬѹ�£��ܶ�֮�ȵ���Ħ������֮�ȣ���������ƽ��Ħ������Ϊ34/2g��mol��1=17g��mol��1�����������ܶ���ͬ��ͬ�R�����º����ܶȵ�17/4=4.25����3����H2�����ʵ���xmol����O2�����ʵ���(2��x)mol������ƽ��Ħ�������Ķ��壬[2x��32(2��x)]/2=17�����x=1�����������ʵ���Ϊ1mol�����������ʵ���Ϊ1mol������2H2��O2=2H2O������״̬�£�H2OΪҺ�壬������ȫ��Ӧ����������0.5mol�����A��B�����֮��Ϊ1��2������ͣ����2����ѹǿ֮�ȵ������ʵ���֮�ȣ���Ϊ1��2��

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�