题目内容
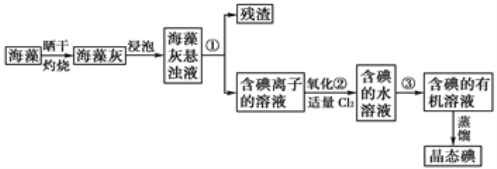
【题目】锌钡白是一种白色颜料。工业上是由ZnSO4与BaS溶液混合而成:BaS+ZnSO4=ZnS↓+BaSO4↓。请根据以下工业生产流程回答有关问题。
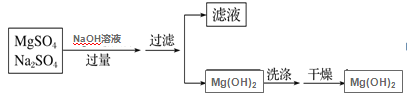
Ⅰ.ZnSO4溶液的制备与提纯:

有关资料:a.菱锌矿的主要成分是ZnCO3,含少量SiO2、FeCO3、Cu2(OH)2CO3等;
b.Zn(OH)2与Al(OH)3相似,能溶于过量的NaOH溶液生成Na2ZnO2。
(1)若②中加入氧化剂为H2O2,写出离子反应方程式____________________________________。
(2)为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤______(选填①、②、③、⑤)。
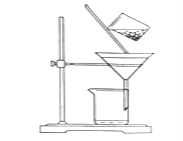
(3)滤渣2的主要成分为_______________________________。
(4)写出步骤④后产生滤渣3的离子反应方程式______________________________。
(5)滤液3中含碳粒子浓度大小的顺序为______________________________________。
Ⅱ.BaS溶液的制备:
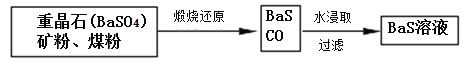
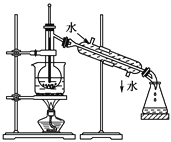
(6)写出煅烧还原的化学反应方程式__________________________________。
BaSO4和BaCO3的KSP相当,解释为什么BaCO3可溶于盐酸中而BaSO4难溶___________________。
Ⅲ.制取锌钡白:
(7)如果生产流程步骤⑤硫酸过量,则ZnSO4与BaS溶液混合制取锌钡白产生的后果是________。
【答案】 2Fe2+ + 2H+ + H2O2 ==2Fe3+ + 2H2O ① Fe(OH)3、Cu(OH)2 ZnO22-+2CO2+2H2O=Zn(OH)2↓+2HCO3- HCO3->H2CO3>CO32- BaSO4 +4C![]() BaS+4CO↑ BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中 过量的酸与BaS溶液混合会产生有毒的H2S污染空气,而且会降低锌钡白的产率
BaS+4CO↑ BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中 过量的酸与BaS溶液混合会产生有毒的H2S污染空气,而且会降低锌钡白的产率
【解析】菱锌矿成分ZnCO3,SiO2、FeCO3、Cu2(OH)2CO3①加硫酸后反应生成ZnSO4、FeSO4、CuSO4,SiO2不溶,形成滤渣1;②加入氧化剂二价铁被氧化为三价铁,其他微粒不变;③加入过量NaOH,生成Fe(OH)3、Cu(OH)2、Na2ZnO2,Fe(OH)3、Cu(OH)2形成滤渣2;④通入过量CO2后反应生成Zn(OH)2、NaHCO3,所以滤渣3即为Zn(OH)2加硫酸后生成ZnSO4。
(1)加入氧化剂二价铁被氧化为三价铁,若②中加入氧化剂为H2O2,反应的离子方程式为2Fe2+ + 2H+ + H2O2 ==2Fe3+ + 2H2O,故答案为:2Fe2+ + 2H+ + H2O2 ==2Fe3+ + 2H2O;
(2)因步骤①中,硫酸与ZnCO3、FeCO3、Cu2(OH)2CO3反应时均产生CO2,为了达到综合利用、节能减排的目的,上述流程步骤④中的CO2可以来自于步骤①,故答案为:①;
(3)根据上述分析,滤渣2的主要成分为Fe(OH)3、Cu(OH)2,故答案为:Fe(OH)3、Cu(OH)2;
(4)由题目信息知:Zn(OH)2与Al(OH)3相似,则与Na2ZnO2与NaAlO2类似,即Na2ZnO2与过量CO2反应方程式为:Na2ZnO2+2CO2+2H2O=Zn(OH)2↓+2NaHCO3,离子方程式为;ZnO22-+2CO2+2H2O=Zn(OH)2↓+2HCO3-故答案为:ZnO22-+2CO2+2H2O=Zn(OH)2↓+2HCO3-;
(5)滤液3的主要成分为碳酸氢钠,碳酸氢钠水解程度大于电离程度,溶液显碱性,含碳粒子浓度大小的顺序为HCO3->H2CO3>CO32-,故答案为:HCO3->H2CO3>CO32-;
(6)根据示意图,硫酸钡与碳粉煅烧还原反应生成BaS和CO,反应的化学反应方程式为BaSO4 +4C![]() BaS+4CO↑,BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中,故答案为:BaSO4 +4C
BaS+4CO↑,BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中,故答案为:BaSO4 +4C![]() BaS+4CO↑;BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中;
BaS+4CO↑;BaCO3溶解出的CO32-能被H+结合而减少,促使溶解平衡正向移动,而SO42-不会被H+结合,所以BaSO4不会溶于强酸中;
(7)如果Ⅰ中步骤⑤使用硫酸过量,会发生如下反应,BaS+H2SO4=H2S↑+ZnSO4,H2S气体有毒,会污染环境,故答案为:过量的酸与BaS溶液混合会产生有毒的H2S气体污染空气,而且锌钡白的产率会降低。

【题目】滴定实验是化学学科中最重要的定量实验之一。常见的滴定实验有酸碱中和滴定、氧化还原反应滴定、沉淀滴定等等。
(1)酸碱中和滴定——用0.1000mol/LHCl标准溶液测定某NaOH溶液的物质的量浓度(用酚酞作指示剂),做了三组平行实验,数据记录如下:
实验序号 | 待测NaOH溶液的体积/mL | 0.1000mol/LHCl溶液的体积/mL | |
滴定前刻度 | 滴定后刻度 | ||
1 | 25.00 | 0.00 | 25.01 |
2 | 25.00 | 1.56 | 26.56 |
3 | 25.00 | 0.21 | 25.20 |
计算出待测NaOH溶液的物质的量浓度为_____________________________(小数点后保留四位)。
(2)氧化还原滴定——葡萄酒中抗氧化剂残留量的测定,葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

注:实验中加入盐酸的目的是将Na2S2O5全部转化成SO2;滴定过程中发生的反应是:I2 + SO2 + 2H2O ![]() 2HI + H2SO4
2HI + H2SO4
①滴定时,I2溶液应装在__________(“酸”或“碱”)式滴定管中,判断滴定终点的方法是:当滴入最后一滴碘溶液时,溶液由_________________________,且保持30s不变。
②实验消耗标准I2溶液25.00mL,所测样品中抗氧化剂的残留量(以游离SO2计算)为___________g/L。
③下列情形会造成测定结果偏高的是_____________。
A.滴定持续时间稍长,溶液中部分HI被空气氧化 B.滴定前平视,滴定后俯视
C.盛装标准I2溶液的滴定管用蒸馏水洗净后,未润洗
D.滴定前滴定管尖嘴有气泡,滴定后气泡消失
(3)沉淀滴定——滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是_____________(填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4