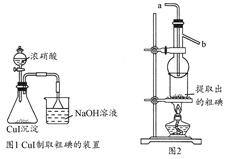
题目内容
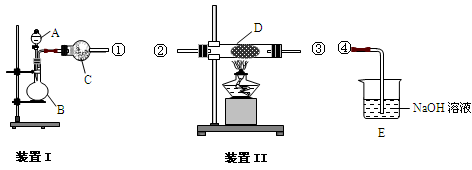
实验室用装置Ⅰ制氨气和氧气的混合气体,A中装有浓氨水,C中盛有碱石灰;用装置Ⅱ
验证氨的某些性质,D内放置催化剂(铂石棉),按气流方向①→②→③→④连接各仪器。
请回答下列问题:
(1)①仪器A的名称是 ,仪器B中应加入的固体药品 (填化学式);
②实验中观察到D内红棕色气体的化学式为 ,证明氨气具有 性;
(2)若用装置Ⅰ制取干燥的SO2气体,则:
①B中发生反应的化学反应方程式为 ;
②此时仪器C中改为盛装P2O5 的作用是 。
验证氨的某些性质,D内放置催化剂(铂石棉),按气流方向①→②→③→④连接各仪器。

请回答下列问题:
(1)①仪器A的名称是 ,仪器B中应加入的固体药品 (填化学式);
②实验中观察到D内红棕色气体的化学式为 ,证明氨气具有 性;
(2)若用装置Ⅰ制取干燥的SO2气体,则:
①B中发生反应的化学反应方程式为 ;
②此时仪器C中改为盛装P2O5 的作用是 。
(1)①分液漏斗; Na2O2 ; ②NO2 ; 还原性
(2)①Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2↑②干燥SO2气体
(2)①Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2↑②干燥SO2气体
试题分析:(1)①根据题意,装置Ⅰ中产生的是氨气和氧气,所以可以加入Na2O2固体;②含氮的化合物只有NO2为红棕色气体,氨气被氧化为二氧化氮,所以氨气表现了还原性 ;(2)①根据强酸制弱酸的原理,反应为:Na2SO3 + H2SO4 = Na2SO4 + H2O + SO2↑②P2O5通常用作酸性干燥剂。

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
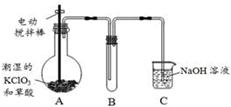
 2MgO+C,请填写以下空白:
2MgO+C,请填写以下空白: