��Ŀ����
��21�֣���ҵ��һ���ں����ܱ���������H2��CO����ȼ�ϼ״�����Ӧ����ʽΪ
CO��g��+2H2��g��CH3OH��g����H
��1���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250��C | 300��C | 350��C |
| K | 2��041 | 0��270 | 0��012 |
���ɱ��������жϡ�H 0���>������=����<����
��ij�¶��£���2molCO��6molH2����2L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c��CO��=0.2mol/L����CO��ת����Ϊ ����ʱ���¶�Ϊ ��
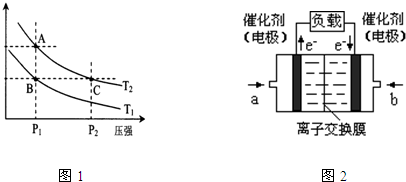
��2����100�� ѹǿΪ0.1 MPa������,�ݻ�ΪV Lij�ܱ�������a mol CO�� 2a mol H2�ڴ��������·�Ӧ���ɼ״�����ƽ��ʱCO��ת����Ϊ50%����100��÷�Ӧ�ĵ�ƽ�ⳣ��K= (�ú�a��V�Ĵ���ʽ��ʾ�������������ʽ)����ʱ�����¶��ݻ����䣬���������г���a mol CH3OH��g����ƽ��_____��������Ӧ�������淴Ӧ�����ƶ����ٴδﵽ��ƽ��ʱ��CO��������� ������С�������䣩
��3��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
A������ B��������� C������CO��Ũ��
D�����ݳ���H2 E����ѹ����������� F��������״�
��4���жϷ�Ӧ�ﵽƽ��״̬�������ǣ�����ĸ��ţ���ͬ�� ��
A������CH3OH������������CO���������
B�����������ܶȲ���
C�������������ƽ��������������
D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��5��300��C�����ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ����й��������£�
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1molCO��2moL H2 | 1molCH3OH | 2molCH3OH | |
| ƽ �� ʱ �� �� �� | CH3OHŨ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | akJ | bkJ | ckJ | |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 |
��ѡ����ȷ�������գ�������ѡ��
��1��c1��c2��c3�Ĺ�ϵ������ȷ��Ϊ______
A c3>2c1 B c1<c3<2c1 C c1=c2
��2��a��b��c�Ĺ�ϵ������ȷ��Ϊ________
A c<2|��H| B a+b=|��H| C c=2b
��3��p1��p2��p3�Ĺ�ϵ����ȷ��Ϊ________
A p1=p2 B p2<p3<2p2 C p3>2p2
��4��a1��a2��a3�Ĺ�ϵ���ﲻ��ȷ��Ϊ________
A a1=a2 B a3< a2 C a1+a2=1
��1����< ��1�֣� �� 80%��2�֣� 250�棨2�֣�
��2��V 2��a2 ��2�֣� ���淴Ӧ����1�֣� ��С��1�֣�
��3��DF ��2�֣� ��4��CD��2�֣�
��5��AC��2�֣� AB��2�֣� C ��2�֣� A��2�֣�
����:

 CH3OH��g����H
CH3OH��g����H