��Ŀ����
�ף��ң�����������������ˮ�����ʣ��ֱ���NH4����Ba2����Mg2����H����OH����Cl����HCO3����SO42���еIJ�ͬ�����Ӻ������Ӹ�һ����ɡ���֪���ٽ�����Һ�ֱ��������������ʵ���Һ��ϣ����а�ɫ�������ɣ��� 0��1mol/L����Һ��c��H����>0��1mol/L���� �����Һ�е���AgNO3��Һ�в�����ϡHNO3�İ�ɫ�������ɡ����н��۲���ȷ���ǣ� ��
| A������Һ���� Ba2�� | B������Һ����SO42�� |
| C������Һ����Cl�� | D������Һ����Mg2�� |
D
����������������ݢ��е���Ϣ��֪���Ƕ�Ԫ�ᣬ������H2SO4�����ݢ�����������֪���к���Cl-���ٽ�Ϣ����ṩ��Ϣ�����������������ʻ�Ͼ�������ɫ����������Ƴ�����Ba��OH��2������H2SO4������MgCl2������NH4HCO3����ѡD��
���㣺����Ϊ�ƶ��⣬����ʱע�����еķ�Ӧ�����ҳ�ͻ�ƿڣ�ץס���ʵ������ǹؼ���

��ϰ��ϵ�д�
 ��������ϵ�д�
��������ϵ�д�
�����Ŀ
���и�������һ���ܴ����������
A��ij��ɫ����������Һ��Cl����Na+��MnO4-�� |
B����ʹpH��ֽ������ɫ����Һ��Na+��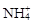 ��K+�� ��K+��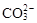 |
| C���������NaOH��Һ��ɵõ��������Һ��K+��Ba2+��HCO3-��Cl�� |
| D����ˮ���������c(H+)=10?12mol/L����Һ��K+��Ba2+��Cl����NO3�� |
�������ӷ���ʽ��д��ȷ����
| A�����Ȼ��ϡ��Һ�м���ϡ�ռ���Һ NH4+ + OH��=NH3��+ H2O |
| B����ˮ�����ᷴӦ H+ + OH��=H2O |
| C���ƺ�ˮ��ӦNa+ 2H2O= Na+ + 2OH��+ H2�� |
| D���������ռ���Һ��ӦCl2+ 2OH��=Cl��+ ClO��+ H2O |
�������ӷ���ʽ������ȷ���ǣ� ����
| A�����Ȼ�����Һ�еμ�HI��Һ��2Fe3++ 2HI = 2Fe2++2H++I2 |
B����NH4Al��SO4��2��Һ�е���Ba��OH��2ǡ��ʹSO42����Ӧ��ȫ��2Ba2++4OH��+Al3++2SO42��=2BaSO4��+AlO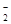 +2H2O +2H2O |
| C��1mol/L��NaAlO2��Һ��2.5 mol/L��HCl��������Ȼ�ϣ�2AlO2����5H+ = Al(OH)3��+Al3+��H2O |
| D���ù���������ữ�ĺ����ҽ���Һ����ȡ��:2I-+H2O2=I2+2OH-�� |
�������ӷ���ʽ��ȷ����
| A����ˮ����������SO2���壺OH��+SO2=HSO3�� |
| B��ϡ�����м���������ۣ� Fe + 4H��+ NO3��=Fe3��+ NO�� + 2H2O |
| C����NaOH��Һ���շ����е������NO+NO2+OH��=NO2��+H2O |
D����������Һ��ͨ������CO2��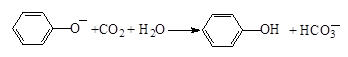 |
�������ӷ���ʽ��������ʵ�������ȷ����
| A����ϡ��ˮ����μ���ϡ��������Һ����������Һ��Ag++2NH3��H2O="[Ag" (NH3)2] ++2 H2O |
| B����˫��ˮ��ϡ�������ʴ��ӡˢ��·�壺Cu+H2O2+2H+=Cu2++2H2O |
C���ؾ�������ˮ��S2��+2H2 O 2OH��+H2S 2OH��+H2S |
| D������ʯ��ˮ������մ���Һ��ϣ�Ca2++2OH��+2HCO3��=CaCO3��+CO32��+2H2O |
�������ӷ���ʽ��ȷ����
| A��������þ��ϡ���ᷴӦ��H+ + OH��=H2O |
| B��AlCl3��Һ�м���������ˮ��Al3����3OH��=Al(OH)3�� |
| C��ͭ����ϡ���3Cu+8H++2NO3��=3Cu2++2NO��+4H2O |
| D�����������Һ��ͨ�����CO2��Ca2++2ClO��+H2O+CO2=CaCO3��+2HClO |
����Һ���ܴ��������һ�����ӻ������
| A��K+ ��Al3+��SO42����NH3��H2O | B��NH4+��H+��NO3����HCO3�� |
C��Na+ ��CH3COO����CO32����OH�� | D��Na+��K+��SO32����Cl2 |
������ط�Ӧ�����ӷ���ʽ��д��ȷ����
| A������������������Fe(OH)3+3H+ = Fe3++3H2O |
| B������ͭ��Һ�����ԣ�Cu2+ + 2H2O = Cu(OH)2��+ 2H+ |
C����̼�������Һ�мӹ���ʯ��ˮ�����ȣ�NH4++OH-  NH3��+H2O NH3��+H2O |
| D�����ữ�ĸ��������Һ����˫��ˮ��2MnO4-+6H++5H2O2 = 2Mn2++5O2��+8H2O |