题目内容
【题目】能用启普发生器制取的气体是( )
A.氢气B.氨气C.氧气D.乙炔
【答案】A
【解析】
A.实验室制取氢气是用锌粒和盐酸反应制取,锌粒是块状的,且此反应不需加热,符合启普发生器的要求,故A正确;
B.实验室制取氨气是用固体氯化铵和固体氢氧化钙加热制取,不能用启普发生器,故B错误;
C.实验室制取氧气可以用高锰酸钾固体受热分解、氯酸钾受热分解或双氧水用二氧化锰做催化剂分解来制取,但无论是哪种方法均不能用启普发生器,故C错误;
D.乙炔的制取是用碳化钙和饱和食盐水反应制取,但由于碳化钙接触水后立即变为糊状,不再是块状固体,故不能用启普发生器,故D错误。
故选:A。

【题目】高锰酸钾[KMnO4]是常用的氧化剂.工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4].图1是实验室模拟制备的操作流程: 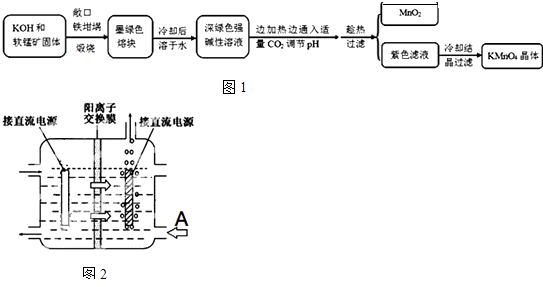
相关资料:
①物质溶解度
物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42﹣)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42﹣会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是;
(2)实验时,若CO2过量会生成KHCO3 , 导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:;
其中氧化还原反应中氧化剂和还原剂的质量比为 .
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中 , 得到的产品纯度更高.
A.醋酸
B.浓盐酸
C.稀硫酸
(4)工业上采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图).图2中A口加入的溶液最好为 . 使用阳离子交换膜可以提高Mn元素利用率的原因为 .
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、 NH4+、 Mg2+、 Ba2+、 Cl-、 SO42—、 CO32—。
将该混合物溶于水后得澄清溶液。 现取3份100 mL该溶液分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
A | 加 AgNO3溶液 | 有白色沉淀生成 |
B | 加足量 NaOH 溶液并加热 | 收集到气体 1.12 L(标准状况下) |
C | 加足量 BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥称量 | 第一次称量沉淀质量为6.63 g,第二次称量沉淀质量为4.66 g |
试回答下列问题:
(1)根据实验A判断 Cl-是否存在_____(填“一定存在” 、 “一定不存在” 或“不能确定”)。
(2)该混合物中一定不存在的离子是_____。
(3)写出实验B发生反应的离子方程式_____________。
(4)溶液中一定存在的阴离子及其物质的量浓度为(可不填满):
阴离子符号 | 物质的量浓度(mol·L-1) |
(5)混合物中是否存在 K+?_____(填“存在” 或“不存在” )
①如果存在, c(K+) _____mol/L(如果选择“不存在” ,此问不必做答)
②如果不存在,判断的理由是_____。(如果选择“存在” ,此问不必做答)