题目内容
【题目】如图所示,下列叙述正确的是 ( )
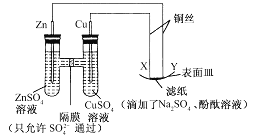
A. Y与滤纸接触处有氧气生成
B. X为正极,发生还原反应
C. SO42-从右侧透过隔膜迁移到左侧
D. X与滤纸接触处变红
【答案】C
【解析】该装置中,左边装置是原电池,Zn易失电子作负极、Cu作正极,右边装置是电解池,X为阳极、Y为阴极,阳极上电极反应为Cu-2e-=Cu2+、阴极电极反应式为2H2O+2e-=2OH-+H2。A.Y电极反应式为2H2O+2e-=2OH-+H2↑,所以Y与滤纸接触处有氢气生成,故A错误;B.X为阳极,失电子发生氧化反应,故B错误;C.在原电池中,阴离子向负极移动,因此SO42-从右侧透过隔膜迁移到左侧,故C正确;D.X电极反应式为Cu-2e-=Cu2+,所以X和滤纸接触处不变红,故D错误;故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是25 ℃时某些弱酸的电离平衡常数。
化学式 | CH3COOH | HClO | H2CO3 | H2C2O4 |
Ka | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ka1=5.9×10-2 Ka2=6.4×10-5 |
(1)H2C2O4与含等物质的量的KOH的溶液反应后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为__________。
(2)pH相同的NaClO和CH3COOK溶液,其溶液的物质的量浓度的大小关系是CH3COOK________NaClO,两溶液中:[c(Na+)-c(ClO-)]________[c(K+)-c(CH3COO-)](填“>”“<”或“=”)。
(3)向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH)∶c(CH3COO-)=5∶9,此时溶液pH=________。
(4)取10 mLpH=2的CH3COOH溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中![]() 的比值将________(填“增大”“减小”或“无法确定”)。
的比值将________(填“增大”“减小”或“无法确定”)。
(5)向碳酸钠溶液中滴加少量氯水的离子方程式为____________________。


