题目内容
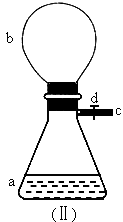
图中瓶a内放入20mL 6mol/L盐酸,b是未充气的气球,里边放有4 g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶侧口,并用弹簧夹d夹紧,(瓶口和侧面都不漏气),将图(Ⅰ)的装置在托盘天平上称量,质量为w g,根据实验现象填写下列空白:
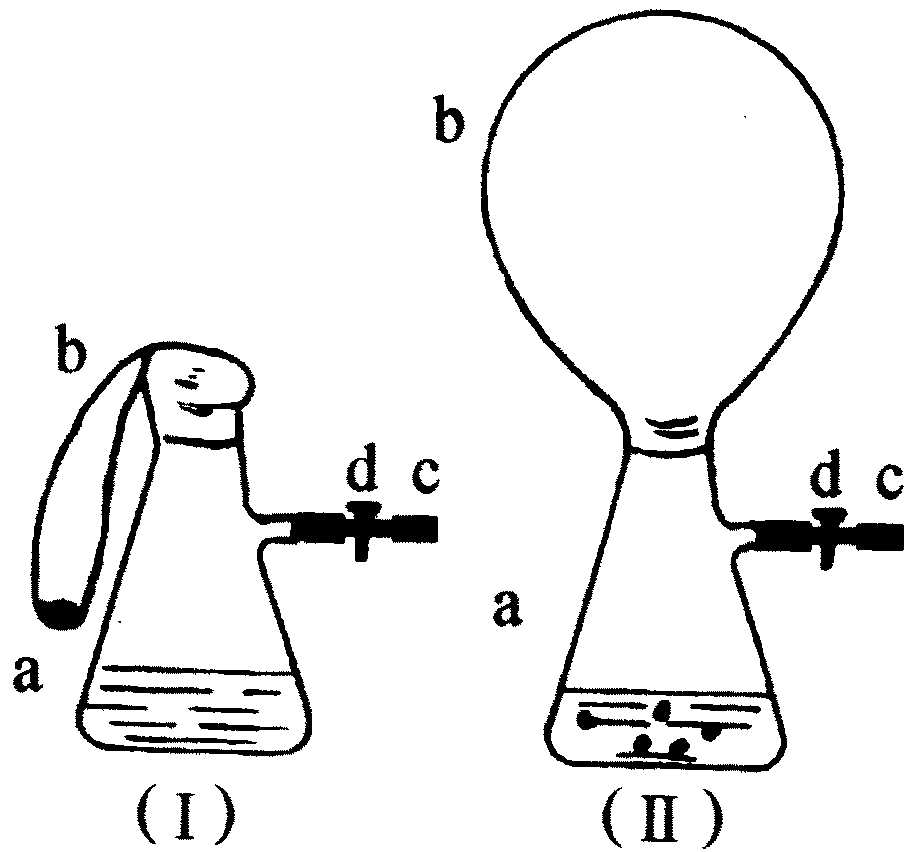
(1)把气球b中CaCO3粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ).反应结束后,再次称量,质量为w2g,则w2和w1的关系是________.
(2)取25 mL 6mol/L NaOH溶液.先用滴管取少量NaOH溶液,滴管插入胶管c口(为便于操作,可以适当倾斜瓶a,注意防止漏气)打开d,将溶液挤入瓶中,立即夹紧d,可以看到瓶内产生少量的白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样的方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失.使沉淀消失的反应的化学方程式是________.
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,此时瓶内温度________(填“不变”、“降低”或“升高”).
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状.写出这时发生的反应的化学方程式________.
答案:
解析:
解析:
|
(1)w1=w2 (2)Ca(OH)2+2HCl=CaCl2+2H2O (3)升高 (4)2NaOH+CO2=Na2CO3+H2O Ca(OH)2+CO2=CaCO3↓+H2O |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

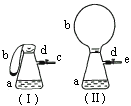
 根据实验现象填写下列空白:
根据实验现象填写下列空白: .(不考虑空气浮力的影响),则
.(不考虑空气浮力的影响),则 和
和 的关系是_______.
的关系是_______.

 根据实验现象填写下列空白:
根据实验现象填写下列空白: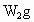 .(不考虑空气浮力的影响),则
.(不考虑空气浮力的影响),则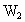 和
和 的关系是_______.
的关系是_______.