题目内容
能说明0.1 mol·L-1的NaHA溶液一定呈酸性的是
①稀释时,溶液中c(OH-)增大 ②溶液的pH<7 ③溶液中c(Na+)=c(A2-) ④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
①稀释时,溶液中c(OH-)增大 ②溶液的pH<7 ③溶液中c(Na+)=c(A2-) ④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
| A.①②③④ | B.①③④ | C.①③ | D.②④ |
C
①分析知NaHA溶液不可能呈中性,溶液呈碱性(或酸性),稀释时溶液的碱性(或酸性)都应该减弱,现溶液中c(OH-)增大,则溶液中c(H+)减小,酸性减弱,故溶液呈酸性;②因温度不确定,故pH<7的溶液不一定呈酸性;③溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),现c(Na+)=c(A2-),故c(H+)=c(OH-)+c(HA-)+c(A2-),所以溶液中c(H+)>c(OH-),溶液呈酸性;④NaHA+NaOH=Na2A+H2O,两者1:1能恰好反应,但并不能确定NaHA溶液呈酸性还是碱性。

练习册系列答案
 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案
相关题目
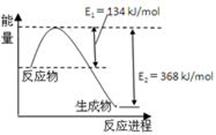
 N2(g)+2CO2(g)的△H是______。
N2(g)+2CO2(g)的△H是______。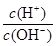 =10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( )
=10-12。将这两种溶液等体积混合后,所得溶液里各离子的物质的量浓度的关系正确的是( ) )+c(Fe2+)+c(H+)=c(OH-)+c(
)+c(Fe2+)+c(H+)=c(OH-)+c( )
) )=c(
)=c( )+3c(H2CO3)+2c(H+)
)+3c(H2CO3)+2c(H+)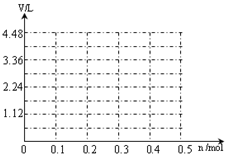 ’
’