题目内容
已知HNO3(浓)和S加热生成NO2,该反应的含硫产物肯定不可能是( )
| A、H2S | B、SO2 | C、SO3 | D、H2SO4 |
分析:HNO3(浓)和S加热生成NO2,反应中N元素化合价降低,硝酸钡还原,则S应被氧化,S元素化合价应升高,以此解答.
解答:解:HNO3(浓)和S加热生成NO2,反应中N元素化合价降低,硝酸钡还原,则S应被氧化,S元素化合价应升高,可能生成SO2、SO3或H2SO4,化合价不可能降低而生成H2S,
故选A.
故选A.
点评:本题易硝酸的性质为载体考查氧化还原反应,注意从元素化合价的角度解答该题,把握反应的特点,特别是化合价的变化规律,难度不大.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目


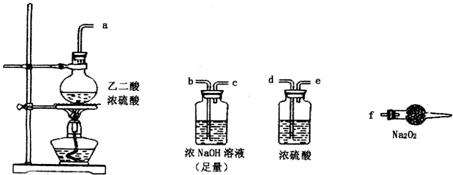
 有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题:
有两个实验小组的同学探究一氧化碳、二氧化硫与过氧化钠的反应.请回答下列问题: