题目内容
8.下列无色溶液中,能大量共存的一组离子是( )| A. | K+、Na+、OH${\;}^{_}$、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$ | |
| B. | Ca2+、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$、Cl-、NH${\;}_{4}^{+}$ | |
| C. | MnO${\;}_{4}^{-}$、Fe2+、Fe3+、Cu2+、SiO${\;}_{3}^{2-}$ | |
| D. | NO${\;}_{3}^{-}$、H+、Fe2+、SO${\;}_{4}^{2-}$、I- |
分析 无色溶液时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.氢氧根离子与碳酸氢根离子反应;
B.四种离子之间不反应,都是无色离子;
C.高锰酸根离子、铜离子、铁离子、亚铁离子都是有色离子;且铁离子、亚铁离子、铜离子都与硅酸根离子反应;
D.硝酸根离子在酸性条件下能够氧化亚铁离子、碘离子,亚铁离子为有色离子.
解答 解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、等有色离子的存在,
A.OH-、HCO3-之间发生反应,在溶液中不能大量共存,故A错误;
B.Ca2+、HCO3-、NO3-、Cl-、NH4+之间不反应,都是无色离子,在溶液中能够大量共存,故B正确;
C. Cu2+、Fe2+、Fe3+、MnO4-都是有色离子,Cu2+、Fe2+、Fe3+都与SiO32-反应发生双水解反应,在溶液中不能大量共存,故C错误;
D.Fe2+为有色离子,NO3-、H+具有强氧化性,能够氧化Fe2+、I-,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
16.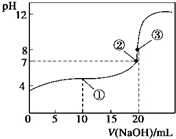 常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )
 常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1 NaOH溶液滴定20.00mL 0.1000mol•L-1 CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )| A. | ①所示溶液中:c(Na+)═c(CH3COOH)+c(CH3COO-) | |
| B. | ②所示溶液中:c(Na+)═c(CH3COO-) | |
| C. | ③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中可能出现:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
3.下列说法错误的是( )
| A. | 蒸馏法分离混合物时,冷凝管下口进水,上口出水 | |
| B. | 分离CCl4和H2O的混合物时,CCl4从分液漏斗下口放出 | |
| C. | 蒸干NaCl溶液制NaCl晶体 | |
| D. | 不能用酒精萃取碘水中的I2 |
20.A、B、C、D、E五瓶透明溶液,分别是BaCl2、Na2CO3、NaHSO4、Ba(OH)2和NaHCO3溶液中的一种.为了鉴别,各取少量溶液进行两两混合,实验结果如下表所示.表中“↓”表
示生成沉淀或微溶化合物,“-”表示观察不到明显现象,“↑”表示有气体产生.
试回答下列问题:
(1)B是Ba(OH)2 C是NaHCO3 D是Na2CO3E是BaCl2(填化学式).
(2)写出下列离子反应方程式
①A与E反应的离子方程式:Ba2++SO42-=BaSO4↓;
②将B的溶液逐滴加入C的溶液中直至过量,在此过程中,所发生的离子反应可能有:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O,Ba2++CO32-=BaCO3↓;
③将等物质的量浓度、等体积的A、B两溶液混合Ba2++OH-+H++SO42-=BaSO4↓+H2O.
示生成沉淀或微溶化合物,“-”表示观察不到明显现象,“↑”表示有气体产生.
| A | B | C | D | E | |
| A | - | ↓ | ↑ | ↑ | ↓ |
| B | ↓ | - | ↓ | ↓ | - |
| C | ↑ | ↓ | - | - | - |
| D | ↑ | ↓ | - | - | ↓ |
| E | ↓ | - | - | ↓ | - |
(1)B是Ba(OH)2 C是NaHCO3 D是Na2CO3E是BaCl2(填化学式).
(2)写出下列离子反应方程式
①A与E反应的离子方程式:Ba2++SO42-=BaSO4↓;
②将B的溶液逐滴加入C的溶液中直至过量,在此过程中,所发生的离子反应可能有:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O,Ba2++CO32-=BaCO3↓;
③将等物质的量浓度、等体积的A、B两溶液混合Ba2++OH-+H++SO42-=BaSO4↓+H2O.
17.锑(Sb)在自然界一般以硫化物的形式存在,我国锑的蕴藏量占世界第一.从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原:①2Sb2S3+3O2+6Fe═Sb4O6+6FeS;②Sb4O6+6C═4Sb+6CO.下列说法正确的是( )
| A. | 反应②说明高温下Sb还原性比C强 | |
| B. | 反应①②中氧化剂分别是Sb2S3、Sb4O6 | |
| C. | 每生成1 mol Sb时,反应①与反应②中还原剂的物质的量之比为1:1 | |
| D. | 反应①中每生成1 mol FeS时,共转移2mol电子 |
 E.
E.