题目内容
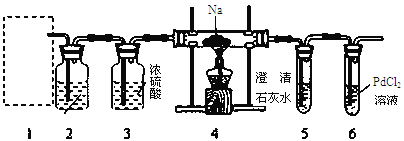
【题目】氮化锂(Li3N)常用作固体电解质和催化剂,遇水蒸气反应生成氢氧化锂和氨气,以一瓶氮气样品(含一氧化碳和氧气)制备纯净的氮化锂,其装置如图所示:
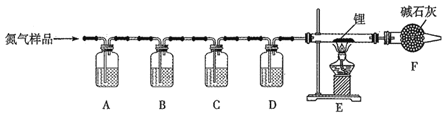
已知:连苯三酚的碱性溶液能吸收少量O2;氯化亚铜的盐酸溶液能吸收少量CO且易被O2氧化。请回答下列问题:
(1)选择下列试剂填入指定位置:
装置代号 | A | B | C | D |
试剂代号 | _____ | ______ | ____ | ____ |
![]() 浓硫酸
浓硫酸 ![]() 氯化亚铜的盐酸溶液
氯化亚铜的盐酸溶液
![]() 连苯三酚的碱性溶液
连苯三酚的碱性溶液 ![]() 氢氧化钠溶液
氢氧化钠溶液
(2)F装置的作用是______________。
(3)实验中,先通入氮气,后点燃酒精灯,目的是_____________。
(4)写出E中反应的化学方程式 ____________。
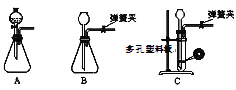
(5)设计如下装置测定产品纯度:称取a g产品于G烧瓶中,向安全漏斗中加入足量蒸馏水,收集到V mL气体(折合成标准状况)。

①安全漏斗的作用是______________________。
②H装置所装液体可能是________________![]() 填字母
填字母![]() 。
。
![]() 饱和氯化铵溶液
饱和氯化铵溶液 ![]() 煤油
煤油 ![]() 饱和食盐水
饱和食盐水 ![]() 苯
苯
③根据上述数据计算,该氮化锂产品纯度为___________。
【答案】c b d a 防止空气中的水蒸气和二氧化碳进入E装置 排尽装置内空气,避免空气中水蒸气和二氧化碳与Li反应产生杂质 N2+6Li![]() 2Li3N 起液封作用
2Li3N 起液封作用 ![]()
![]()
【解析】
由实验装置可知,A中连苯三酚碱性溶液能定量吸收O2,B中氯化亚铜盐酸溶液能定量吸收CO,c中NaOH溶液吸收其中的CO2,D中浓硫酸干燥氮气,E中发生N2+6Li![]() 2Li3N,且Li3N遇水蒸气剧烈反应生成氢氧化锂和氨气,F中无水氯化钙或碱石灰可吸收空气中水,防止进气E中,以此来解答。
2Li3N,且Li3N遇水蒸气剧烈反应生成氢氧化锂和氨气,F中无水氯化钙或碱石灰可吸收空气中水,防止进气E中,以此来解答。
(1)由题意可知:A中放连苯三酚的碱性溶液吸收氧气,B中放氯化亚铜的盐酸溶液吸收一氧化碳,C中放氢氧化钠溶液吸收氯化氢,D中放浓硫酸干燥,故合理选项序号分别是c;b;d;a;
(2)F装置用于防止空气中水蒸气和二氧化碳进入E装置,避免水蒸气和二氧化碳与装置内锂或氮化锂反应;
(3)装置内空气中物质能与锂反应实验中,加热前必须排尽空气,所以先通入氮气,后点燃酒精灯,目的是排尽装置内空气,避免空气中水蒸气和二氧化碳与Li反应产生杂质;
(4)在装置E中,锂与氮气化合生成氮化锂,反应方程式为:N2+6Li![]() 2Li3N ;
2Li3N ;
(5)①安全漏斗中加入液体,能起到液封作用,避免气体从漏斗中逸出;
②用排液法收集氨气,说明氨气不溶于该液体,由于氨气极容易溶于水,所以饱和氯化铵溶液、饱和食盐水不能使用,排除选项ac;液体可能是煤油和苯,故合理选项是bd;
③Li3N与H2O反应产生LiOH、NH3,反应方程式为:Li3N+3H2O=3LiOH+NH3,根据方程式可知:n(Li3N)=n(NH3),n(NH3)=![]() =
=![]() mol,所以氮化锂产品纯度为
mol,所以氮化锂产品纯度为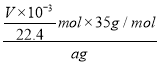 ×100%=
×100%=![]() %。
%。