题目内容
【题目】下列说法中正确的是
A.对于乙酸与乙醇的酯化反应(ΔH<0),加入少量浓硫酸并加热,该反应的反应速率与平衡常数均增大
B.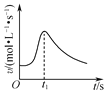 如图是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高
如图是镁条与盐酸反应的化学反应速率随反应时间变化的曲线,说明t1时刻溶液的温度最高
C.反应2HI(g)H2(g)+I2(g),达到平衡后,缩小容器容积可使体系颜色变深。该现象不能用勒夏特列原理解释
D.若反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)在常温下能自发进行,则该反应的ΔH>0
【答案】C
【解析】
A.浓硫酸作催化剂、吸水剂,加热可加快反应速率,但正反应为放热反应,加热,平衡逆向移动,则该反应的反应速率增大,而平衡常数减小,故A错误;
B.镁条与盐酸反应的化学反应速率随反应时间变化的曲线,开始时,反应放热,温度升高,反应速率加快,但随浓度减小,一段时间后反应速率减小,t1时刻溶液的温度不一定最高,故B错误;
C.对于2HI(g)H2(g)+I2(g),达平衡后,缩小容器体积,压强增大,平衡不移动,但I2浓度变大,颜色变深,该现象不能用勒夏特列原理解释,故C正确;
D.生成物只有固体,△S<0,若该反应能自发进行,根据△H-T△S<0,则△H必须小于0,故D错误;
故选C。

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目