��Ŀ����
����A��E�������±��е�������ɵģ������½������ʵ���
Һ��1 mLϡ�͵�1 000 mL��pH�ı仯��ϵ��ͼ����ʾ������A��D��Ӧ�õ�E����ش��������⡣
| ������ | NH4+��H����Na�� |
| ������ | OH����CH3COO����Cl�� |

(1)����pH�ı仯��ϵ��д�����ʵĻ�ѧʽ��B ��C ��
(2)д��A��C��Ӧ�����ӷ���ʽ�� ��
(3)ͼ��Ϊ����ʱ��25 mLijŨ�ȵ�B��Һ����εμ�0.2 mol��L��1��D��Һ�Ĺ�����pH�ı仯���ߡ�
��ͼ����B�����ʵ���Ũ��Ϊ mol��L��1��
��G����Һ�����ԣ������ǡ����ȫ��Ӧ�ĵ�����FG���仹��GH���䣿 ���䡣
��FG������Һ�и�����Ũ�ȴ�С��ϵ�� ��
(4)t ��ʱ��A��ϡ��Һ��c(H��)��10��a mol��L��1��c(OH��)��10��b mol��L��1����֪a��b��13�����¶���(t ��)����100 mL 0.2 mol��L��1��C��Һ��100 mL 0.4 mol��L��1��B��Һ��Ϻ�(��Һ����仯���Բ���)����Һ��pH�� ��
(1)NaOH��HCl
(2)NH3��H2O��H��=NH4+��H2O
(3)��0.1����FG
��c(Na��)��c(OH��)��c(CH3COO��)��c(H��)��c(Na��)��c(CH3COO��)��c(OH��)��c(H��)
(4)12
����

��16�֣��Ƽ��仯������й㷺����;��
(1)��ҵ���Ʊ������Ƶij��÷����� (�����ӷ���ʽ��ʾ)��
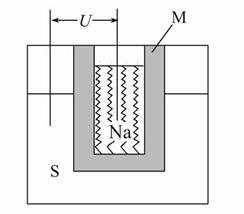
(2)��Na2CO3������������ʣ�CO��O2��CO2Ϊԭ�Ͽ�������͵�ء��õ�صĽṹ��ͼ��ʾ��
�����ĵ缫��ӦʽΪ ����ع���ʱ����A��ѭ��ʹ�ã�A���ʵĻ�ѧʽΪ ��
(3)�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��1����������������Һ��pH���±���
| ���� | CH3COONa | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 11.6 | 10.3 | 11.1 |
a��HCN b��HClO c��CH3COOH d��H2CO3
(4)ʵ�����г���NaOH������β��������ϴ�����ᴿ��
�ٳ����£���300 mL 1 mol��L��1��NaOH��Һ����4.48 L(����ɱ�״��)SO2ʱ��������ҺpH��7������Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
����֪�������ӿ�ʼ����ʱ��pH���±���
| ���� | Fe2�� | Cu2�� | Mg2�� |
| pH | 7.6 | 5.2 | 10.4 |
��һѧ����ʵ���Ҳ�ij��Һ��pH,ʵ��ʱ,����������ˮ��ʪpH��ֽ,Ȼ���ýྻ����IJ�����պȡ�������м��:
(1)��ѧ���IJ�������������(���ȷ�ġ�����ġ�),����������������������������������
(2)���ô˷����ֱ�ⶨc(H+)��ȵ�����ʹ�����Һ��pH,���ϴ������������,ԭ����
������������������������������
(3)��ѧ����������ʽ�ⶨ������Һ��pH,��������(����)
| A��NaOH | B��CH3COONa | C��NaCl | D��NaHSO4 |
��ͼ��ʾ��������Ϊ��Һ��pHֵ��������ΪZn2�����ӻ�Zn(OH)42���������ʵ���Ũ�ȵĶ������ش��������⡣
(1)��ZnCl2��Һ�м�������������������Һ����Ӧ�����ӷ���ʽ�ɱ�ʾΪ��________��
(2)��ͼ�����ݼ���ɵ�Zn(OH)2���ܶȻ�(Ksp)��________��
(3)ij��Һ�к�Zn2�����ӣ�Ϊ��ȡZn2�����ӿ��Կ�����Һ��pHֵ�ķ�Χ��________________________��
(4)��֪����ZnCl2��Һ�м�������Ǧ�����Ǧ��Һ�����Ƶ�PbCl2��ɫ���壻25��ʱ��PbCl2�����������е��ܽ�����£�
| c(HCl)/( mol��L��1) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| c(PbCl2)/( mol��L��1)��10��3 | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
�����ϱ������ж�����˵����ȷ����________(����ĸ���)��
A����������Ũ�ȵ�����PbCl2������ܽ���ȱ�С���ֱ��
B��PbCl2������0.50 mol��L��1�����е��ܽ��С���ڴ�ˮ�е��ܽ��
C��PbCl2����Ũ���ᷴӦ����һ���ѵ����������(���������)
D��PbCl2��������ڱ���ʳ��ˮ
�±��Dz�ͬ�¶���ˮ�����ӻ������ݣ�
| �¶�/�� | 25 | t1 | t2 |
| ˮ�����ӻ� | 1��10��14 | a | 1��10��12 |
�Իش��������⣺
(1)��25��t1��t2����a________1��10��14(�����������������)�������жϵ�������_______________________________________________________��
(2)25 ��ʱ��ijNa2SO4��Һ��c(SO42��)��5��10��4 mol��L��1��ȡ����Һ1 mL��ˮϡ����10 mL����ϡ�ͺ���Һ��c(Na��)��c(OH��)��________��
(3)��t2�¶��²��ij��ҺpH��7������Һ��________(��ᡱ��������С�)�ԣ������¶���pH��11��NaOH��Һa L��pH��1��H2SO4��Һb L��ϣ������û��ҺpH��2����a��b��________��
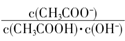 ����
���� ��С
��С

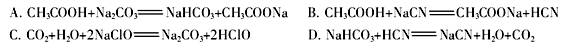

 ���ӵ���Һ�еμ�NaOH��Һʱ�� �������ӷ��ţ��ȳ�����
���ӵ���Һ�еμ�NaOH��Һʱ�� �������ӷ��ţ��ȳ����� �����������������������
�����������������������