题目内容
(1)物质的量浓度相同的三种盐NX、NaY、NaZ的溶液,其pH依次为8、9、1 0,则HX、HY、HZ的酸性由强到弱的顺序是 。
(2)比较下列溶液的pH(填“>”“<”或“=”):
①0.1 mol·L-1Na2CO3溶液 0.1 mol·L-1NaHCO3溶液
②0.1 mol·L-1NH4Cl溶液 0.01 mol·L-1NH4C1溶液
(3)把a、b、c、d四块金属片浸泡在稀H2SO4中,用导线两两相连,可以组成各种原电池。若a、b相连,a为负极;c、d相连,c为负极;a、c相连,c为正极;b、d相连,b为正极,则这四种金属的活动性由强到弱的顺序为 。
(4)将AlCl3溶液蒸干、灼烧,最后所得的固体的主要成份是 。
(5)氯化铁溶液呈 性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,溶液的pH 7(填“>”“<”或“=”),离子反应总方程式为: 。
(1)HX>HY>HZ(2)>;< (3)a>c>d>b(4)氧化铝(5)酸Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
(6)Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O
解析试题分析:(1)因pH越大,说明酸根离子水解越是强烈,对应的酸越弱,所以HX、HY、HZ的酸性由强到弱的顺序:HX>HY>HZ
(2) ①同浓度的Na2CO3和NaHCO3溶液,CO32-水解程度大于 HCO3-所以0.1 mol·L-1Na2CO3溶液 > 0.1 mol·L-1NaHCO3溶液②不同浓度的NH4Cl溶液浓度越小,NH4+水解程度越大,但是水解后溶液的酸性越弱。所以②0.1 mol·L-1NH4Cl溶液 < 0.01 mol·L-1NH4C1溶液.
(3) 组成各种原电池。若a、b相连,a为负极;活动性a>b, c、d相连,c为负极;c>d; b、d相连,b为正极d>b,综上:a>c>d>b. (4) AlCl3溶液蒸干得到氢氧化铝,灼烧得到氧化铝。(5) 氯化铁溶液呈酸性,因为Fe3+水解。Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
(6)向明矾溶液中逐滴加入Ba(OH)2溶液至SO42-刚好沉淀完全时,发生的反应如下Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O.得到的是NaAlO2溶液,溶液的pH<7.
考点:盐类的水解的应用和金属活动性比较

已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液;a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是_______________(用编号填写)。
(2)常温下,0.1mol·L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
A.c(H+ )
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-)
D.c(OH-)/c(H+)
E.c(H+)·c(CH3COO-)/c(CH3COOH)
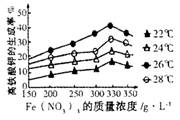
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如下图所示,则同温度时HX的电离平衡常数_ ____(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是_____________________。

(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精确值)。
(5)标准状况下,将1.12L CO2通入100mL 0.75mol·L-1的NaOH溶液中,则溶液中离子的浓度由大到小的顺序
有A、B、C、D四种强电解质,它们在水中电离可产生表中离子(每种物质只含一种阴离子且互不重复)。
| 阳离子 | Na+、Ba2+、NH4+ | 阴离子 | CO32-、Cl-、OH-、SO42- |
②C溶液和D溶液相遇时只观察到有白色沉淀产生,B溶液和C溶液相遇时只观察到有刺激性气味的气体产生,A溶液和D溶液混合时无明显现象。请填写下列空白:
(1)A是___________,B是___________,C是____________,D是___________。
(2)常温,将1 ml pH =12的C溶液加水稀释至100ml,所得溶液中
 = ;
= ;(3)常温下,0.15 mol·L-1的C溶液与0.20 mol·L-1盐酸混合,所得混合液的pH=13,则C溶液与盐酸的体积比= _______________。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序是 。


 Sr2+(aq)+SO42-(aq) Ksp=2.5×10-7
Sr2+(aq)+SO42-(aq) Ksp=2.5×10-7