题目内容
【题目】实验题:将V1 mL 1.0molL﹣1HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始保持V1+V2=50mL).请按要求填空:

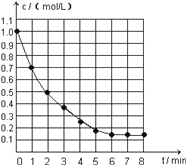
(1)该实验表明此反应 (填吸收、释放)能量,即: 能可以转化为 能,通过甲图示分析可以得出:做该实验时,环境温度 (填高于、低于、等于)22℃;
(2)根据甲图示计算该NaOH溶液的浓度约是 molL﹣1
(3)如图乙所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:
①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体
其中能使a端液面高于b端液面的是 .(填序号)
【答案】(1)释放;化学;热;低于;(2)1.5;(3)③
【解析】
试题分析:(1)根据示意图,溶液的温度升高,说明该反应为放热反应,释放能量,化学能转化为热能,根据示意图,反应5分钟时,溶液温度升高至22℃,所以做该实验时,环境温度低于22℃。
(2)根据V1+V2=50mL,根据示意图,加入盐酸30mL时,NaOH溶液的体积为20mL,溶液的温度最高,说明二者恰好反应,则30×10-3L×1.0molL1=20×10-3L×c(NaOH),则c(NaOH)=1.5molL1。
(3)如果a端液面高于b端液面,说明锥形瓶内气体体积减小,则温度降低,向小试管内加入的物质发生吸热过程,硝酸铵溶于水吸热,故答案为③。

【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32- |
实验I :取少量该试液进行如下实验。

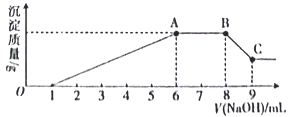
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液,向该溶液中滴加1 mol L-l的 NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。
回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有___________种。
(2)通过实验I可以确定该溶液中一定存在的阴离子是_____________。检验气体X的方法是______________________;沉淀Z的化学式为_________________。
(3)写出实验Ⅱ的图象中BC段对应的离子方程式:_____________________________________。
(4) A点对应的固体质量为__________g。
(5)通过上述信息,推算该溶液中阴离子的浓度为______________mol L-l。