题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,22.4LNO和11.2LO2混合后气体的分子总数为NA
B. 标准状况下,由H2O2制得4.48LO2转移的电子数目为0.8NA
C. 14g由乙烯与环丙烷组成的混合气体含有的碳原子数目为NA
D. 25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0.1NA
【答案】C
【解析】
A、22.4LNO标准状况下,合1mol,O2的物质的量为0.5mol,NO与O2发生2NO+O2=2NO2,NO和O2恰好完全反应,但2NO2![]() N2O4,因此反应后气体物质的量小于1mol,故A错误;B、转移电子物质的量为
N2O4,因此反应后气体物质的量小于1mol,故A错误;B、转移电子物质的量为![]() mol=0.4mol,故B错误;C、乙烯分子式为C2H4,环丙烷的分子式为C3H8,符合通式为CnH2n,14g混合气体含有碳的物质的量为
mol=0.4mol,故B错误;C、乙烯分子式为C2H4,环丙烷的分子式为C3H8,符合通式为CnH2n,14g混合气体含有碳的物质的量为![]() mol=1mol,故C正确;D、题目中没有说明溶液的体积,无法计算OH-的物质的量,故D错误。
mol=1mol,故C正确;D、题目中没有说明溶液的体积,无法计算OH-的物质的量,故D错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
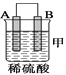
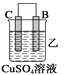
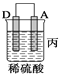
【题目】由A、B、C、D四种金属按下表中装置进行实验。
装置 |
|
|
|
现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中作正极的是__________________ (填“A”或“B”) ;
(2)装置乙溶液中C电极反应:__________________________________;装置乙中反应一段时间后,测得C电极 的质量增加12.8克,则该电池反应转移电子的物质的量为___________mol
(3)装置丙中金属A上电极反应属于______________(填“氧化反应”或“还原反应”);
(4)四种金属活动性由强到弱的顺序是_______________________。