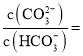题目内容
【题目】石灰石是一种化工原料,可以通过反应生成一系列物质,如图::

下列说法正确的是( )
A.漂粉精是混合物,主要成分是氯化钙
B.图示的制纯碱方法,要求先向饱和食盐水中通NH3,,然后再通CO2
C.纯碱属于碱,俗名苏打
D.制取纯碱和漂粉精所涉及的反应都是非氧化还原反应
【答案】B
【解析】
A.根据工业流程图判断漂白精的主要成分;
B.NH3极易溶于水且溶液呈弱碱性,再通入CO2使之更多地转化为HCO3;
C.碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;
D.制备漂白精的反应中氯元素的化合价发生变化,属于氧化还原反应。
A.漂白精为氯气和氢氧化钙反应的产物,2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,其主要成分是次氯酸钙和氯化钙,故A错误;
B.NH3极易溶于水且溶液呈弱碱性,再通入CO2使之更多地转化为HCO3,故工业上,可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3,碳酸钠受热分解制取纯碱,故B正确;
C.纯碱是碳酸钠,俗名苏打,是由钠离子和碳酸根离子组成的化合物,属于盐,故C错误;
D.向饱和食盐水中通NH3,然后再通CO2制取碳酸氢钠,加热分解碳酸氢钠制取纯碱,两反应中元素化合价不变化,属于非氧化还原反应,但制备漂白精的反应中氯元素的化合价由0价变化为1、+1价,属于氧化还原反应,故D错误;
故答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目