题目内容
【题目】(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___(填字母)。
a.![]() b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
b.CH4 c.CH2=CHCH3 d.CH3CH2C≡CH
(2)BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为___,B与N之间形成___键。硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质。[B(OH)4]-中B的原子杂化类型为___,不考虑空间构型,[B(OH)4]-的结构可用示意图表示为___。
(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。
①“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。已知N2O分子中氧原子只与一个氮原子相连,则N2O的电子式可表示为___,其分子立体构型是___形。
②另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl2):2CHCl3+O2→2HCl+2COCl2,光气(COCl2)分子的立体构型是___形。
(4)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图所示。
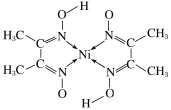
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是___,氮镍之间形成的化学键是___。
②该结构中,碳原子的杂化轨道类型有___。
【答案】d sp3 配位 sp3 ![]()
![]() 直线 平面三角 一个σ键,一个π键 配位键 sp2、sp3
直线 平面三角 一个σ键,一个π键 配位键 sp2、sp3
【解析】
(1)①饱和C原子采取sp3杂化,双键C原子和苯环C原子采取sp2杂化,三键C原子采取sp杂化,故答案为:d;
(2)B原子的价电子排布式为2s22p1,BF3分子中B原子采取sp2杂化,B原子有一个未参与杂化的2p空轨道,NH3分子中N原子有一对孤电子对,N与B原子之间形成配位键;BF3·NH3中,B原子与3个F原子和1个N原子以单键结合形成4个σ键,故B原子采取sp3杂化;[B(OH)4]-中B原子相连的σ键数为4,因此B的原子杂化类型为sp3;B原子最外层电子数为3,与3个OH-成键,B原子有1个空轨道,OH-提供孤电子对形成配位键,不考虑空间构型,[B(OH)4]-的结构可用示意图表示为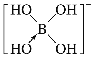 ;
;
(3)①因氧原子只与一个氮原子相连,利用每个原子最外层8e-稳定结构可写出其电子式为![]() ;中间氮原子价层电子对数为2,孤电子对数为0,故N2O为直线形;
;中间氮原子价层电子对数为2,孤电子对数为0,故N2O为直线形;
②COCl2的结构式为![]() ,碳原子形成1个π键和3个σ键,故碳原子采取sp2杂化,COCl2为平面三角形分子;
,碳原子形成1个π键和3个σ键,故碳原子采取sp2杂化,COCl2为平面三角形分子;
(4)①单键为σ键,双键中有1个σ键和1个π键,所以碳氮之间的共价键是1个σ键和1个π键;氮原子提供孤电子对,Ni原子提供空轨道,形成配位键;
②—CH3中的C原子形成4个σ键,C原子采取sp3杂化,含双键的C原子形成3个σ键,C原子采取sp2杂化。

【题目】镁、铝、铁及其化合物在生产和生活中有广泛的应用。
(1)镁铝合金用在飞机制造业,现有3.90克镁铝合金溶于足量的2mol/L稀硫酸中生成0.2mol氢气,计算并确定镁铝合金中物质的量n(Mg): n(Al)=________。
(2)硫铁矿的主要成分为FeS2(假设杂质只含SiO2)是生产硫酸的原料。取某硫铁矿10g在足量的空气中煅烧(4FeS2+11O2=2Fe2O3+8SO2),充分反应后冷却,称得固体质量为7.4g(杂质SiO2不反应)。该硫铁矿中FeS2的质量分数为_____。
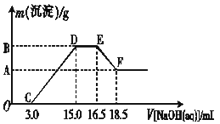
(3)现有一定量的铁粉和铝粉组成的混合物跟100 mL稀硝酸充分反应,反应过程中无任何气体放出,往反应后的澄清溶液中逐渐加入4.00 mol·L-1的NaOH溶液,加入NaOH溶液的体积与产生沉淀的质量的关系如图所示(必要时可加热,忽略气体在水中的溶解),纵坐标中A点的数值是________。
(4)炼铁厂生产的生铁常用于炼钢。取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,得到CO2气体224mL(标准状况下)。
①计算此钢样粉末中铁和碳的物质的量之比为________________(最简单的整数比)。
②再取三份不同质量的上述钢样粉末分别加到100mL相同浓度的稀H2SO4中,充分反应后,测得的实验数据如下表所示:
实验序号 | Ⅰ | Ⅱ | Ⅲ |
加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
则该硫酸溶液的物质的量浓度为__________________。
③若在上述实验Ⅱ中继续加入m克钢样粉末,计算反应结束后剩余的固体质量为___g(保留3位小数)。