题目内容
【题目】(1)含苯酚的工业废水必须处理达标后才能排放,苯酚含量在1 g·L-1 以上的工业废水应回收苯酚。某研究性学习小组设计下列流程,探究废水中苯酚的回收方法。
![]()
①可用_______为试剂检验水样中是否含有苯酚。
②操作I的名称为_______,试剂a的化学式为_______。
③通入CO2发生反应生成苯酚的化学方程式为________。
(2)某有机物的分子式为C3H6O3。
①1 mol该有机物充分燃烧消耗的O2在标准状况下的体积为_________L。
②若两分子该有机物能生成六元环状结构,写出该反应的化学方程式_________。
【答案】 FeCl3溶液或浓溴水 萃取(或萃取分液) NaOH C6H5ONa+CO2+H2O→C6H5OH+NaHCO3 67.2 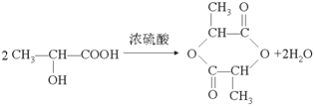
【解析】(1)①苯酚与氯化铁发生显色反应,苯酚与溴水反应生成白色沉淀,则选择检验试剂为FeCl3溶液或浓溴水,故答案为:FeCl3溶液或浓溴水;
②由分离流程可知,加苯为萃取剂,操作I为萃取,然后得到有机层;苯酚与NaOH反应生成苯酚钠溶于水,则试剂a为NaOH,故答案为:萃取(或萃取分液);NaOH;
③苯酚钠与二氧化碳、水反应生成苯酚、碳酸氢钠,该反应为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,故答案为:C6H5ONa+CO2+H2O→C6H5OH+NaHCO3;
(2)①1mol该有机物(C3H6O3)充分燃烧生成CO2和H2O,消耗O2为3+![]() -
-![]() =3mol,在标准状况下的体积为3mol×22.4L/mol=67.2L,故答案为:67.2;
=3mol,在标准状况下的体积为3mol×22.4L/mol=67.2L,故答案为:67.2;
②有机物两分子间相互反应生成含有六元环状结构的产物,说明分子结构含有羟基和羧基,发生酯化反应,该反应为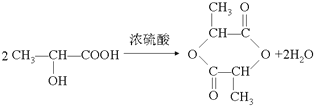 ,故答案为:
,故答案为: 。
。

练习册系列答案
相关题目