题目内容
下列除去杂质所选用的试剂或方法完全正确的是( )
| A、除去NaCl溶液中的少量I2:用无水乙醇,萃取分液 |
| B、除去CO2中少量HCl:通入饱和Na2CO3溶液,洗气 |
| C、除去NaHCO3固体中少量Na2CO3:加热灼烧 |
| D、除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.乙醇与水混溶,不能作萃取剂;
B.二者均与碳酸钠反应;
C.加热碳酸氢钠分解;
D.Fe与氯化铁反应生成氯化亚铁.
B.二者均与碳酸钠反应;
C.加热碳酸氢钠分解;
D.Fe与氯化铁反应生成氯化亚铁.
解答:
解:A.乙醇与水混溶,不能作萃取剂,则应用苯或四氯化碳,萃取分液来除杂,故A错误;
B.二者均与碳酸钠反应,应利用饱和NaHCO3溶液,洗气来除杂,故B错误;
C.加热碳酸氢钠分解,将原物质反应掉,不符合除杂的原则,故C错误;
D.Fe与氯化铁反应生成氯化亚铁,则加入足量铁屑,充分反应后,过滤可除杂,故D正确;
故选D.
B.二者均与碳酸钠反应,应利用饱和NaHCO3溶液,洗气来除杂,故B错误;
C.加热碳酸氢钠分解,将原物质反应掉,不符合除杂的原则,故C错误;
D.Fe与氯化铁反应生成氯化亚铁,则加入足量铁屑,充分反应后,过滤可除杂,故D正确;
故选D.
点评:本题考查物质分离、提纯方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,注意混合物分离方法的选择和除杂的原则,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
除去下列物质中所含少量杂质(括号内),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 甲烷(乙烯) | 溴水 | 洗气 |
| B | 蔗糖(葡萄糖) | 银氨溶液 | 过滤 |
| C | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
| D | 淀粉胶体(氯化钠溶液) | 蒸馏水 | 过滤 |
| A、A | B、B | C、C | D、D |
下列说法正确的是( )
| A、1mol Cl2与足量NaOH溶液反应转移电子的物质的量为2mol |
| B、用含有0.2mol HCl的浓盐酸与足量MnO2加热后,可制得1.12LCl2(标况) |
| C、向新制氯水中通入SO2,氯水的漂白能力将增强 |
| D、向新制氯水中加入CaCO3,溶液中有气泡放出 |
下列说法正确的是(其中NA表示阿伏伽德罗常数)( )
| A、常温常压下,0.1mol 2H216O中含中子数、质子数、电子数均为NA |
| B、比黄金还贵的18O2和普通的16O2是两种不同的核素 |
| C、标准状况下,2.24L Cl2溶于水,转移的电子数目为0.1NA |
| D、1L 2mol?L-1的Al(NO3)3溶液中含Al3+个数为2NA |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、
| ||
| B、1.0mol?L-1 KNO3溶液:H+、Fe2+、Cl-、SO42- | ||
| C、含有0.1mol?L-1 Ca2+溶液:Na+、K+、CO32-、Cl- | ||
| D、澄清透明的溶液:Na+、K+、MnO4-、[Al(OH)4]- |
加热固体试剂时,不能使用的仪器是( )
| A、试管 | B、烧杯 | C、燃烧匙 | D、坩埚 |
有10g不纯CaCO3样品与足量盐酸作用后生成4.44g CO2,且溶液中残留难溶物质.则对于此样品中是否存在①MgCO3②K2CO3③SiO2杂质的判断正确的是( )
| A、肯定含①③,不含② |
| B、肯定含①③,可能含② |
| C、肯定含②③,不含① |
| D、肯定含②③,可能含① |
常温下,向100mL盐酸中滴加NaOH溶液,溶液的PH变化如图,由图可得出的正确结论是( )
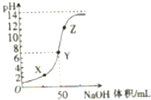

| A、原来盐酸的物质的量浓度为0.1 mol?L-1 |
| B、Y处溶液中只有两种离子 |
| C、原NaOH溶液的物质的量浓度为1 mol?L-1 |
| D、水的电离程度:X>Y>Z |
对于反应3Cl2+6NaOH═5NaCl+NaClO3+3H2O,以下叙述不正确的是( )
| A、NaClO3中Cl的化合价是+5 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量的比为1:5 |
| C、Cl2既是氧化剂又是还原剂 |
| D、每生成1mol的NaClO3转移6mol的电子 |