题目内容
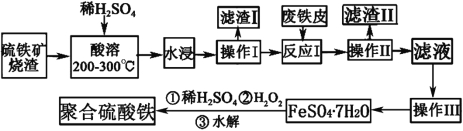
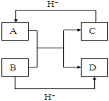
【题目】利用控制n(H2S):n(FeCl3)=1:2反应得到的产物再用电解法制氢,其工作原理如图所示。下列有关的说法错误的是( )
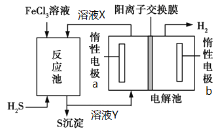
A. 惰性电极a发生氧化反应
B. Fe(OH)3胶体中滴加溶液X,先有沉淀后沉淀溶解
C. 溶液Y加热蒸发灼烧最终得到Fe2O3
D. 电解池总反应的离子方程式为2Fe2++2H+![]() 2Fe3++H2↑
2Fe3++H2↑
【答案】B
【解析】
试题分析:H2S与FeCl3反应生成硫单质和氯化亚铁以及盐酸。A. 根据示意图,惰性电极b放出氢气,说明b为阴极,则a为阳极,发生氧化反应,故A正确;B. 惰性电极a发生氧化反应生成氯气,氯气将氯化亚铁氧化为氯化铁,因此溶液X为氯化铁,Fe(OH)3胶体中滴加氯化铁,发生胶体的聚沉,但不能溶解,故B错误;C. 溶液Y为氯化亚铁,加热蒸发灼烧会被空气中的氧气氧化,最终得到Fe2O3,故C正确;D. 根据AB的分析,电解池总反应的离子方程式为2Fe2++2H+![]() 2Fe3++H2↑,故D正确;故选B。
2Fe3++H2↑,故D正确;故选B。

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目