题目内容
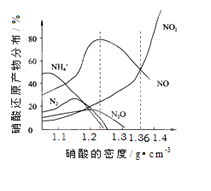
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据图1和图2所示,回答下列问题:

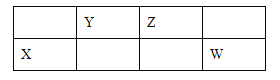
图1
(1)Y的化学式为__________________
(2)欲制备Na2S2O3,从氧化还原角度分析,合理的是______________(填序号)。
a.Na2S +S b.Na2SO3+S c.Na2SO3+Na2SO4 d.SO2+Na2SO4
(3)将X与O2混合,可生成淡黄色固体。该反应的氧化剂与还原剂物质的量之比为_____________。
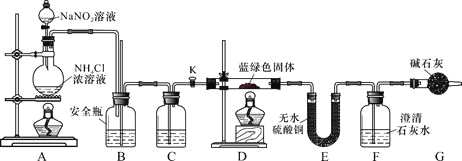
(4)图2为铜丝与W的浓溶液反应并验证其产物性质的实验装置。

图2
Ⅰ.①中反应的化学方程式是_____________。想要立即终止①的反应,最恰当的方法是__________。
a.上移铜丝,使其脱离溶液 b.撤去酒精灯 c.拔去橡胶塞倒出溶液
Ⅱ.④中棉花团的作用是_________________。
Ⅲ.反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式_________________
【答案】 SO2 b 1:2 Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑ a 吸收SO2尾气 SO2+Cl2+2H2O=4H++2Cl-+SO42- Ba2++SO42-=BaSO4↓(SO2+Cl2+2H2O+Ba2+=4H++2Cl-+BaSO4↓)
CuSO4+2H2O+SO2↑ a 吸收SO2尾气 SO2+Cl2+2H2O=4H++2Cl-+SO42- Ba2++SO42-=BaSO4↓(SO2+Cl2+2H2O+Ba2+=4H++2Cl-+BaSO4↓)
【解析】本题考查硫及其化合物的性质,(1)Y对应的是+4价硫的氧化物,即SO2;(2)Na2S2O3中S显+2价,根据氧化还原反应的规律,其中一个硫元素的化合价高于+2价,一个S元素的化合价低于+2价,即选项b正确;(3)根据图1,X为气态氢化物,其中S显-2价,即X为H2S,H2S与氧气反应生成淡黄色固体,即生成S,反应方程式为2H2S+O2=2S+2H2O,H2S中S的化合价升高,H2S作还原剂,O2作氧化剂,因此氧化剂与还原剂的物质的量之比为1:2;(4)W为H2SO4,I.铜和浓硫酸反应,反应方程式为Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑;想要终止反应,让铜丝与浓硫酸不接触,故选项a正确;II.④SO2有毒,必须尾气处理,因此棉花的作用是吸收SO2气体;III.SO2不与BaCl2反应,BaCl2溶液中溶于SO2,SO2+H2O=H2SO3,利用氯气的强氧化性,与H2SO3发生氧化还原反应,即H2O+H2SO3+Cl2+Ba2+=BaSO4↓+2Cl-+4H+,或者是SO2+Cl2+2H2O+Ba2+=4H++2Cl-+BaSO4↓。
CuSO4+2H2O+SO2↑;想要终止反应,让铜丝与浓硫酸不接触,故选项a正确;II.④SO2有毒,必须尾气处理,因此棉花的作用是吸收SO2气体;III.SO2不与BaCl2反应,BaCl2溶液中溶于SO2,SO2+H2O=H2SO3,利用氯气的强氧化性,与H2SO3发生氧化还原反应,即H2O+H2SO3+Cl2+Ba2+=BaSO4↓+2Cl-+4H+,或者是SO2+Cl2+2H2O+Ba2+=4H++2Cl-+BaSO4↓。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案