题目内容
【题目】某化学兴趣小组为了测定某铁碳合金中铁的质量分数,设计了下图所示的实验装置和实验方案(夹持仪器已省略),请你参与此项活动并回答相应问题。
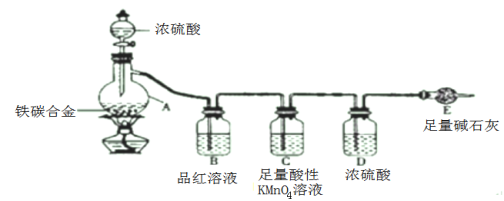
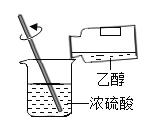
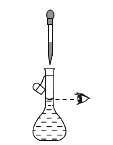
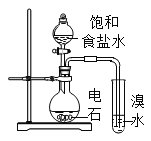
(1)按图示的连接装置,检查装置的气密性并称量E的质量。将10克铁碳合金样品放入A中,再加入适量的浓硫酸,仪器A的名称为_________________。未点燃酒精灯前,A、B均无明显现象 。
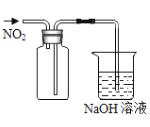
(2)点燃酒精灯一段时间后,A、B中可观察到明显的现象。写出A中浓硫酸参与反应的化学方程式 __________________(任写一个)。C装置的作用是 _____________ 。
(3)反应一段时间后,从A中逸出气体的速率仍然较快,除因温度较高,反应放热外,还可能的原因是_____________________。
(4)待A中不再逸出气体时,停止加热,拆下E并称重。E增重1.1克。则铁碳合金中铁的质量分数为 _________________ 。
(5)该装置存在一些缺陷,使得测定结果可能会产生误差,请指出该装置的缺陷__________ 、 __________________________
【答案】蒸馏烧瓶 ![]() 或
或![]() 或
或![]() 除去二氧化硫 形成了铁碳原电池 97% 没有驱赶残留气体 E装置直接与空气相通,会吸收空气中的二氧化碳和水造成误差。
除去二氧化硫 形成了铁碳原电池 97% 没有驱赶残留气体 E装置直接与空气相通,会吸收空气中的二氧化碳和水造成误差。
【解析】
(1)仪器A为蒸馏烧瓶;
(2)铁碳合金样品放入A中,再加入适量的浓硫酸加热,浓硫酸具有强氧化性和铁在加热条件下反应生成硫酸铁和二氧化硫水;碳和浓硫酸加热反应生成二氧化碳二氧化硫水,依据书写化学方程式的原则写出;装置C的作用是除去二氧化硫;
(3)铁、碳在硫酸溶液中形成原电池,能加快化学反应速率;
(4)根据10g铁碳合金,加入过量浓硫酸,气体通过浓硫酸干燥后通入干燥管E,E中所装试剂为碱石灰,可吸收CO2;E增重1.1g,则生成二氧化碳的质量为1.1g,根据质量守恒定律,则可求出10g铁碳合金中含碳元素的质量进而求出铁的质量分数;
(5)根据空气中的二氧化碳和水蒸气也会进入E装置。
(1)仪器A为蒸馏烧瓶,
故答案为:蒸馏烧瓶;
(2)铁碳合金样品放入A中,再加入适量的浓硫酸加热,浓硫酸具有强氧化性和铁在加热条件下反应生成硫酸铁和二氧化硫水;碳和浓硫酸加热反应生成二氧化碳二氧化硫水,方程式分别为:![]() ,
,![]() ,
,![]() ;装置C的作用是除去二氧化硫,
;装置C的作用是除去二氧化硫,
故答案为:![]() 或
或![]() 或
或![]() ;除去二氧化硫;
;除去二氧化硫;
(3)铁、碳在酸溶液中符合原电池的组成条件,形成原电池反应,能加快化学反应速率;
故答案为:形成了铁碳原电池;
(5)装称取10g铁碳合金,加入过量浓硫酸,加热待A中不再逸出气体时,停止加热,拆下E装置并称重,E增重1.1g,则生成二氧化碳的质量为1.1g,根据质量守恒定律,则10g铁碳合金中含碳元素的质量![]() ,则含铁的质量为9.7g,铁的质量分数
,则含铁的质量为9.7g,铁的质量分数![]() ,
,
故答案为:97%;
(6)该装置缺陷为:没有驱赶残留气体,导致CO2测量不准确,空气中的二氧化碳和水蒸气也会进入E装置,
故答案为:没有驱赶残留气体;E装置直接与空气相通,会吸收空气中的二氧化碳和水造成误差。

 一本好题口算题卡系列答案
一本好题口算题卡系列答案