题目内容
【题目】六氟化硫分子(如下图)呈正八面体,难以水解,在电器工业方面有着广泛用途。下列有关SF6的推测正确的是( )

A.SF6易燃烧生成二氧化硫
B.SF6是极性分子
C.SF6中各原子均达到 8 电子稳定结构
D.高温条件下,SF6微弱水解生成H2SO4和HF
【答案】D
【解析】
F是唯一没有正价的元素,F为-1价,SF6中S元素为+6价,S已处于最高价,不可能再被氧气氧化生成硫为+4价的二氧化硫,故A错误;六氟化硫分子呈正八面体,结构对称,是非极性分子,故B错误;六氟化硫分子呈正八面体,F达到八电子稳定结构,1个F最外层周围有8个电子,1个S最外层周围有12个电子.故C错误;SF6中F为-1价, S为+6价,微弱水解:SF6+4H20=H2SO4+6HF,故D正确。

 阶梯计算系列答案
阶梯计算系列答案【题目】高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。
(资料)K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。
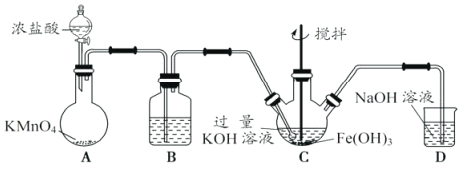
①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为___________。
②除杂装置B中的试剂为___________。
③C为制备K2FeO4装置,KOH溶液过量的原因是___________。
④D为尾气处理装置,发生反应的离子方程式为___________。
(2)探究 K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黃绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
①由方案I中溶液变红可知a中含有___________。该离子的产生___________(填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是___________。方案Ⅱ得出氧化性:Cl2___________FeO42-(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)________。现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为___________。(计算结果保留到0.1%)
【题目】乙酸异戊酯是组成密蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1 .0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
实验步骤:在A中加入4.4g异戊醇![]() 、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液洗涤;分出的产物再加入少量无水Na2SO4固体,静止片刻。过滤除去Na2SO4固体,讲行蒸馏纯化。收集140~143°C馏分,得到乙酸异戊酯3.9g。回答下列问题:
、6.0g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液洗涤;分出的产物再加入少量无水Na2SO4固体,静止片刻。过滤除去Na2SO4固体,讲行蒸馏纯化。收集140~143°C馏分,得到乙酸异戊酯3.9g。回答下列问题:
(1)实验中制备乙酸异戊酯的化学方程式为_________________。
(2)仪器B的名称是_______________,作用是____________。
(3)在洗涤操作中饱和碳酸氢钠溶液的主要作用是______________。
(4)实验中加入少量无水Na2SO4的目的是_________________________。
(5)实验中加过量乙酸的目的是___________________________。
(6)本实验的产率是_______________(填标号)。
a.30% b.40% c.50% d.60%