题目内容
【题目】电解原理在化学工业中有广泛应用。如图示,是一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
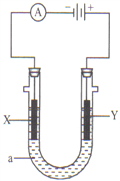
若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时, 同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式是:______________;在X极附近观察到的现象是:__________________。
②Y电极上的电极反应式是:_____________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极的材料是_____;
②Y电极的电极反应式是_____________________。(不考虑杂质反应)
(3)若要在铁钉表面镀铜,X电极的材料是_____。
【答案】 2H++2e-=H2↑(或2H2O+2e-=H2↑+2OH-) 放出气体,溶液变红 2Cl-- 2e- = Cl2↑ 纯铜 Cu-2e-==Cu2+ 铁钉
【解析】(1)①装置图可知X连接电源负极,为电解池阴极,溶液中氢离子得到电子发生还原反应生成氢气,电极反应为:2H++2e-=H2↑,破坏了水的电离平衡,溶液中氢氧根离子浓度增大,酚酞变红色; 则在X极附近观察到的现象是:放出气体,溶液变红;② Y电极连接电源正极,为电解池阳极,溶液中氯离子失去电子发生氧化反应生成氯气,电极反应为:2Cl-- 2e- = Cl2↑;(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:①X连接电源负极,为电镀池的阴极,电极的材料是纯铜;②Y电极为电镀池的阳极,粗铜失去电子产生铜离子,不考虑杂质反应,电极反应式是Cu-2e-=Cu2+;(3)若要在铁钉表面镀铜,X电极上镀铜,材料是铁钉。

【题目】蛋壳的主要成分是CaCO3,含有少量的SiO2、MgCO3及色素等杂质,测定蛋壳中钙含量的操作步骤如图所示:
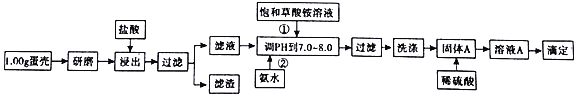
已知:CaC2O4、MgC2O4都难溶于水。
回答下列问题:
(1)样品溶于盐酸后得到的滤渣主要是______________。
(2)①②操作时,加入饱和(NH4)2C2O4溶液和氨水的作用是_________。
(3)洗涤固体A最好选用“冰水”洗涤,其目的是___________。
(4)在一定温度下,向2L的密闭容器中放人足量的草酸钙(固体所占体积忽略不计)发生反应:CaC2O4(s)![]() CaO(s)+CO(g)+CO2(g)若前5min内生成CaO的质量为l1.2g,则该段时间内v(CO)=_________。
CaO(s)+CO(g)+CO2(g)若前5min内生成CaO的质量为l1.2g,则该段时间内v(CO)=_________。
(5)用标准酸性高锰酸钾溶液滴定生成的草酸,通过钙与草酸的定量关系,可间接求出钙的含量。
步骤1:将溶液A加蒸馏水稀释至250mL。
步骤2:取稀释后的溶液25.00mL于锥形瓶中,加稀H2SO4酸化。
步骤3:用0.0190mol/LKMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1mI。
步骤4:重复步骤2、步骤3的操作3次,记录数据如下表:
实验编号 | KMnO4溶液的浓度(mol/L) | KMnO4液滴入的体积(mL) |
1 | 0.0190 | V1=20.02 |
2 | 0.0190 | V2=20.00 |
3 | 0.0190 | V3=19.98 |
4 | 0.0190 | V4=20.80 |
①滴定终点的现象是______________________。
②该蛋壳中CaCO3的质量分数=______%,则此法求得的钙含量_____实际值(填“>”“=”或“<”)。
【题目】生活中为了延长鲜花的寿命,通常会在花瓶中加入鲜花保鲜剂。下表是0.5 L某种鲜花保鲜剂中含有的成分及含量,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(g/mol) |
蔗糖(C12H22O11) | 25.00 | 342 |
硫酸钾(K2SO4) | 0.25 | 174 |
高锰酸钾(KMnO4) | 0.25 | 158 |
阿司匹林(C9H8O4) | 0.17 | 180 |
硝酸银(AgNO3) | 0.02 | 170 |
(1)鲜花保鲜剂的下列成分中,属于电解质的是________(填字母)。
a.蔗糖 b.硫酸钾
c.高锰酸钾 d.硝酸银
(2)欲配制480 mL该鲜花保鲜剂,现已提供下列仪器:
①胶头滴管、②量筒、③烧杯、④药匙、⑤电子天平,如要完成实验,缺少的玻璃仪器还有________(写仪器名称)。
(3)写出该鲜花保鲜剂中K+的物质的量浓度的计算式:________(不必化简)。
(4)将m g蔗糖完全燃烧后的产物通过足量的Na2O2固体,充分反应后,固体增加的质量________(填“>”“=”或“<”)m g。