��Ŀ����
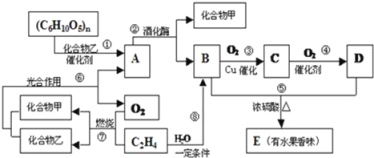
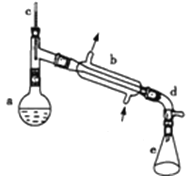
����Ŀ������ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ����ͼ��ʾ�������õ����й��������£�
��Է������� | �ܶ�/��gcm��3�� | �е�/�� | �ܽ��� | |
���Ҵ� | 100 | 0.9618 | 161 | ����ˮ |
����ϩ | 82 | 0.8102 | 83 | ������ˮ |
a�м���20g��������2СƬ���Ƭ����ȴ��������������1mLŨ���ᣮb��ͨ����ȴˮ��ʼ��������a�������������¶Ȳ�����90�森��Ӧ�ֲ��ﵹ��f�зֱ�������5%̼������Һ��ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������õ���������ϩ��
�ش��������⣺
��1���ɻ�������ȡ����ϩ�ķ�Ӧ����Ϊ_________��
��2��װ��b������ˮ������______�����½��ϳ����Ͻ��³�����
��3���������Ƭ��������______���������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������___������ȷ�𰸱�ţ���
A���������� B����ȴ�� C�����貹�� D����������
��4����ʵ���������ײ����ĸ����������Ĺ���������Ϊ____��
��5���ڷ����ᴿ�У�ʹ�õ�������f������_____�������Ȼ��ƵIJ�����_____��
��6���ϳɹ����м���Ũ�����������_____��
���𰸡���ȥ��Ӧ �½��ϳ� ��ֹ���� B �Ѽ� ��Һ©�� ���� ��������ˮ��
��������
(1)���������ɻ���ϩ�����л�����ȥС�������ɷ����к���˫���IJ������л�������2������ˮ�½��ϳ��������������Ч������3�����Ƭ�Ĵ��ڿ��Է�ֹ�ڼ��ȹ����в��������������������Ƭʱ��Ҫ���Ѽ��ȵ���Һ��ȴ���ټ��룻(4)���ȹ����У����������ɷ�����ȥ��Ӧ���ɻ���ϩ�⣬�����Է������Ӽ���ˮ��Ӧ���ɶ�����������5������ϩ������ˮ����Ӧ�ֲ��ﵹ��f�зֱ�������5%̼������Һ��ˮϴ�ӣ�����ϩ��ˮ�ֲ㣬�÷�Һ�������ᴿ���Ȼ����ǹ�������Һ�����ù��˷�����6����������Ũ�������������ˮ���ɻ���ϩ��
(1)���������ɻ���ϩ�����л�����ȥС�������ɷ����к���˫���IJ������л�����������ȥ��Ӧ����2������ˮ�½��ϳ��������������Ч��������װ��b������ˮ�������½��ϳ�����3�����Ƭ�Ĵ��ڿ��Է�ֹ�ڼ��ȹ����в��������������Լ������Ƭ�������Ƿ�ֹ���У��������Ƭʱ��Ҫ���Ѽ��ȵ���Һ��ȴ���ټ��룬��ѡB��(4)���ȹ����У����������ɷ�����ȥ��Ӧ���ɻ���ϩ�⣬�����Է������Ӽ���ˮ��Ӧ���ɶ������ѣ����Ը����������Ĺ���������Ϊ�Ѽ�����5������ϩ������ˮ����Ӧ�ֲ��ﵹ��f�зֱ�������5%̼������Һ��ˮϴ�ӣ�����ϩ��ˮ�ֲ㣬�÷�Һ�������ᴿ������װ��f�Ƿ�Һ©�����Ȼ����ǹ�������Һ�����ù��˷�����6����������Ũ�������������ˮ���ɻ���ϩ��Ũ����������Ǵ�������ˮ����

����Ŀ�������仯����Ի�����������Ӱ�졣
(1)��֪���������е����仯��������·�Ӧ��
![]() ��H=+180 kJ��mol-1
��H=+180 kJ��mol-1
![]() ��H=+68 kJ��mol-1
��H=+68 kJ��mol-1
��![]() ��H=__________ kJ��mol-1
��H=__________ kJ��mol-1
(2)���ڷ�Ӧ![]() �ķ�Ӧ�������£�
�ķ�Ӧ�������£�
��һ����
�ڶ�����![]()
���пɽ�����Ϊ�ڶ�����Ӧ��Ӱ���һ����ƽ�⣬��һ����Ӧ�У�����=k1����c2(NO)������=k1����c(N2O2)��k1����k1��Ϊ���ʳ����������¶�Ӱ�졣����������ȷ����______(����)
A ������Ӧ�������ɵ�һ����Ӧ���ʾ���
B ͬһ�¶��£�ƽ��ʱ��һ����Ӧ��k1����k1��Խ��Ӧ����̶�Խ��
C �ڶ�����Ӧ���ʵͣ����ת����Ҳ��
D �ڶ�����Ӧ�Ļ�ܱȵ�һ����Ӧ�Ļ�ܸ�
(3)��ѧ���о�����һ�ָ�Ч���������Խ�CO��NO2����ת��Ϊ����Ⱦ���壬��Ӧ����ʽΪ��![]() ��H<0��ij�¶��£���10 L�ܱ������зֱ����0��1 mol NO2��0��2 mol CO������������Ӧ�����ŷ�Ӧ�Ľ��У������ڵ�ѹǿ�仯���±���ʾ��
��H<0��ij�¶��£���10 L�ܱ������зֱ����0��1 mol NO2��0��2 mol CO������������Ӧ�����ŷ�Ӧ�Ľ��У������ڵ�ѹǿ�仯���±���ʾ��
ʱ�䣯min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
ѹǿ��kPa | 75 | 73.4 | 71.95 | 70.7 | 69.7 | 68.75 | 68.75 |
�ڴ��¶��£���Ӧ��ƽ�ⳣ��Kp=___________kPa-1(K
(4)����������װ�е���Ԫ��װ�ã���������CO��NO�ȵ���Ⱦ����Ӧ��������
I�� NO+Pt(s)=NO(*) [Pt(s)��ʾ������NO(*)��ʾ����̬NO����ͬ]
��CO+Pt(s)=CO(*)
III��NO(*)=N(*)+O(*)
IV��CO(*)+O(*)=CO2+2Pt(s)
V��N(*)+N(*)=N2+2 Pt(s)
VI��NO(*)+N(*)=N2O+2 Pt(s)
β���з�Ӧ�P������Ũ�����¶ȵı仯��ϵ��ͼ��

��330�����µĵ�������������Ҫ��Ӧ�Ļ�ѧ����ʽ��__________________________��
�ڷ�ӦV�Ļ��_____��ӦVI�Ļ��(�<������>����=��)��������_________________��
����Ŀ��A��B��C��D��EΪԭ��������������Ķ���������Ԫ�أ���ԭ�Ӱ뾶�������������Ĺ�ϵ����ͼ1��Eԭ��������ϵĵ�������Dԭ��������������4����D���Ӻ�������Ų���C2����ͬ��

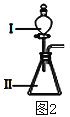
�Իش�
��1��Ԫ��E��Ԫ�����ڱ��е�λ����___________________��
��2����Ԫ��D��������������������������ͬ������________________�����û�ѧʽ������ͬ��
��3��B��E����������Ӧ��ˮ������Խ�����_________________��������ͼ2��װ����֤�������������ǿ��������װ���м�����Լ��ֱ�Ϊ����___________����__________���۲쵽��ʵ��������________________________��
��4������������Ԫ����ɵ����ʣ�����ɺͽṹ��Ϣ���±���
���� | ��ɺͽṹ��Ϣ |
a | ����A��C��D���� |
b | C��D��ɵĻ������ԭ����֮��Ϊ1��1 |
c | ��ѧ���ΪAC2 |
��a���еĻ�ѧ����___________________________________��
��b��c��Ӧ�Ļ�ѧ����ʽΪ_________________________________��