��Ŀ����
����Ŀ����ҵ�ϳ�ͨ�����·ֽ�FeSO4�ķ����Ʊ�Fe2O3��Ϊ����FeSO4���·ֽ�IJ���������й�̽��ʵ�飬�ش��������⣺

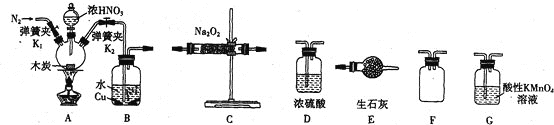
ʵ��һ�����·ֽ�FeSO4��������ͼ1��ʾ��ʵ��װ�ý���ʵ�顣
��֪����SO2�۵�Ϊ-72�棬�е�Ϊ-10�棻��SO3�۵�Ϊ-16.8�棬�е�Ϊ44.8�档
��1������װ�ã��������������ã�����ҩƷ��ͨ��һ��ʱ��N2Ȼ����ȣ�ͨ��N2��Ŀ����___��
��2����������������650�棬����B���а�ɫ������D�Թ�������ɫҺ�壬Ӳ�ʲ������еĹ����Ϊ___��ͬʱ��������ɫ�������ɣ�д���÷�Ӧ�Ļ�ѧ����ʽ___��
��3����Ӧ��Ϻ�ֹͣ������ȴ��ȡӲ�ʲ������й��壬�����ᣬ��Ӧ�����ӷ���ʽ��___������Ӧ��������Һ����D�Թ��У���Һ��Ϊdz��ɫ���÷�Ӧ�����ӷ���ʽ��___��
ʵ�����̽�����·ֽ�FeSO4���ɵ�����
��4������ͼ2��ʾװ�����ʵ�飬��֤���·ֽ�FeSO4���ɵ���̬����
�ٰ������������Ӹ�����������ĸ��ʾ�ӿڵ�����˳��c-___��
���Լ�X��������___��
�۳�ַ�Ӧ������װ�� III��Բ����ƿ�ڻ����ⶨ�ѷֽ��FeSO4����������Բ����ƿ�������Ȼ�����Һ��ֱ��������ȫ��Ȼ����˻����ڹ������Ͻ�����ϴ����ɲ���ȴ�����£����أ������յõ�����������ΪWg�����ѷֽ��FeSO4������__g��
���𰸡��ų�װ���еĿ��� ����ɫ 2FeSO4![]() Fe2O3+SO2��+SO3�� Fe2O3+6H+=2Fe3++3H2O 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ a-b-f-g-d Ʒ����Һ
Fe2O3+SO2��+SO3�� Fe2O3+6H+=2Fe3++3H2O 2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ a-b-f-g-d Ʒ����Һ ![]()
��������
ʵ��һ�����������ڼ��������º����ױ������е�������������������ͬʱ��������ɫ�������ɣ�B���а�ɫ�������ж������������Ϊ������������������ݻ��ϼ۵ĸı䣬����Fe2O3��
ʵ�����Aװ��ΪFeSO4�ڸ����·ֽ�����Fe2O3��SO3��SO2��װ�ã�����������ˮ��Ӧ�������ᣬ���������۵�ߣ������ñ�ˮ�����ʹ��������Һ�����������������Ʒ����Һ�����������ж�������Ⱦ��������Ҫβ��������װ������Բ����ƿ���������������Ȼ���ȫ����Ӧ�������ᱵ���������ݳ���������������������������ʵ�������ϻ�ѧ����ʽ����ֽ����������������
ʵ��һ��![]() �ڼ��������£�������������ױ������е����������������ڼ���֮ǰ��ͨ��
�ڼ��������£�������������ױ������е����������������ڼ���֮ǰ��ͨ��![]() ��Ŀ�����ų�װ���еĿ�����
��Ŀ�����ų�װ���еĿ�����
![]() ���а�ɫ�������ó���Ϊ���ᱵ����������ɫ�������ɣ���ӦΪ�������������������Ԫ�ػ��ϼ۽��ͣ�����Ԫ�ػ��ϼ�����Ϊ����������������ɫ����ѧ����ʽΪ��
���а�ɫ�������ó���Ϊ���ᱵ����������ɫ�������ɣ���ӦΪ�������������������Ԫ�ػ��ϼ۽��ͣ�����Ԫ�ػ��ϼ�����Ϊ����������������ɫ����ѧ����ʽΪ��![]()
![]()
![]() ��
��
��3��.���ݷ���ʽӲ�ʲ������еĹ���Ϊ�������������������ӷ���ʽΪ��![]() ������Ӧ��������Һ����D�Թ��У���Һ�������ӱ���ԭ��dz��ɫ���������ӣ�����������������������ӣ��÷�Ӧ�����ӷ���ʽΪ
������Ӧ��������Һ����D�Թ��У���Һ�������ӱ���ԭ��dz��ɫ���������ӣ�����������������������ӣ��÷�Ӧ�����ӷ���ʽΪ![]() ��
��
ʵ�����
(4)��װ��IΪ![]() �ڸ����·ֽ�����
�ڸ����·ֽ�����![]() ��
��![]() ��
��![]() ��װ�ã�����������ˮ��Ӧ�������ᣬ���������۵�ߣ������ñ�ˮ�����ʹ��������Һ������c��a�������������������Ʒ����Һ��������װ��Ʒ����Һ����b��f���������������ж�������Ⱦ��������������������Һ���գ���g��d������˳��Ϊ
��װ�ã�����������ˮ��Ӧ�������ᣬ���������۵�ߣ������ñ�ˮ�����ʹ��������Һ������c��a�������������������Ʒ����Һ��������װ��Ʒ����Һ����b��f���������������ж�������Ⱦ��������������������Һ���գ���g��d������˳��Ϊ![]() ��
��
![]() �������Ư���ԣ���ʹƷ����Һ��ɫ����װ������װ��Ʒ����Һ�����������������ɣ�
�������Ư���ԣ���ʹƷ����Һ��ɫ����װ������װ��Ʒ����Һ�����������������ɣ�
![]() װ�����еõ���������������һϵ�й������յõ�����Ϊ���ᱵ,����������ΪWg
װ�����еõ���������������һϵ�й������յõ�����Ϊ���ᱵ,����������ΪWg
������Ԫ���غ��ϻ�ѧ����ʽ������ϵ��֪��
![]()
2 1
![]()
�ѷֽ��������������Ϊ��

����Ŀ����ʽ̼��ͭ[Cu(OH)2CuCO3]��һ����;�㷺�Ļ�����Ʒ��ʵ�����Ʊ���ʽ̼��ͭ�ķ�Ӧԭ��Ϊ��2CuSO4+2Na2CO3+H2O=Cu(OH)2CuCO3��+CO2��+2Na2SO4���ش��������⣺
��1������100mLŨ�Ⱦ�Ϊ0.50molL-1��CuSO4��Һ��Na2CO3��Һ����Ҫ�õ��IJ�����������Ͳ���ձ�����ͷ�ιܺ�___��
��2��ȡ50mL0.50molL-1CuSO4��Һ����50mL0.50molL-1Na2CO3��Һ�У���Ӧ���ձ��ײ����ִ�������ɫ���������ʵ��֤������ɫ�����л���������ˮ�ļ�ʽ����ͭ[Cu2(OH)2SO4]��ʵ�鲽���ǣ����ˣ�___��
��3���������� n(CuSO4)�Un(Na2CO3)=1�U1.2����ʵ�飬��Ӧ15min������ʵ�������£�
�¶�/�� | 60 | 65 | 75 | 80 | 90 |
������/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
����75��ʱ����������ԭ��___��
��4���������Ͽ�֪��ʽ̼��ͭ������ж��֣�����xCu(OH)2yCuCO3��ʾ��ijС����������װ�òⶨij��ʽ̼��ͭ��Ʒ����ɣ�
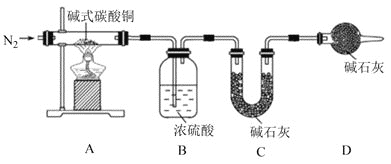
��A�з�����Ӧ�Ļ�ѧ����ʽ��___��
�ڼ���ʱ����ͨ��N2��Ŀ����___��
�۳�ȡ32.0g��Ʒ����ַ�Ӧ��õ�24.0g�����B����3.6g��C����4.4g������Ʒ�Ļ�ѧʽΪ___�����Ե�B��Cװ�õ�λ�ã�___(������������������)���������Ʒ�Ļ�ѧʽ��