题目内容
某些建筑材料含有放射性元素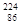 Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是
Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是
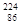 Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是
Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是| A.52 | B.138 | C.86 | D.224 |
A
试题分析:
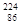 Rn质子数是86,中子数是224-86=138.所以该原子的中子数和质子数之差是138-86=52.选项为A。
Rn质子数是86,中子数是224-86=138.所以该原子的中子数和质子数之差是138-86=52.选项为A。
练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
题目内容
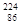 Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是
Rn(氡),会对人体产生一定危害。该原子的中子数和质子数之差是| A.52 | B.138 | C.86 | D.224 |
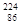 Rn质子数是86,中子数是224-86=138.所以该原子的中子数和质子数之差是138-86=52.选项为A。
Rn质子数是86,中子数是224-86=138.所以该原子的中子数和质子数之差是138-86=52.选项为A。
 优加精卷系列答案
优加精卷系列答案