题目内容
【题目】某课外活动小组对甲酸进行了如下的实验,以验证其含有醛基,并考察其化学性质。首先做了银镜反应:
(1)取少量甲酸加入NaOH溶液中和其酸性,反应的离子方程式为_________________。
(2)在(1)的溶液中加入足量银氨溶液,加热,产生了银镜。甲酸钠溶液与银氨溶液发生银镜反应的离子方程式为_______________________________________________。
(3)某同学很成功的做了银镜反应,他肯定没有进行的操作_________________(写字母):
A.用洁净的试管 B.向银氨溶液中加入硝酸酸化
C.用前几天配制好的银氨溶液 D.直接在银氨溶液里加入稍过量的甲酸;
E.在浓度为2%的NH3H2O中滴入稍过量的浓度为2%的硝酸银
然后,同学们对甲酸与甲醇的酯化反应进行了研究:
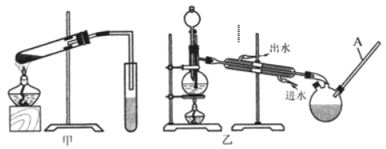
(4)写出![]() 和CH3-18OH进行酯化反应的化学方程式______________________。
和CH3-18OH进行酯化反应的化学方程式______________________。
(5)你认为选择甲装置还是乙装置好?_______,原因是______________________。乙装置中长导管C的作用是_________________。
(6)实验中饱和碳酸钠溶液的作用是_____________________________。从饱和碳酸钠溶液中分离出酯需要用到的主要实验仪器是_______________。
(7)一同学用装有饱和氢氧化钠的三颈烧瓶接收甲酸甲酯,几乎没有收集到产物,请给予合理的解释_______________________________。
【答案】NaOH+HCOOH=HCOONa+H2O HCOO-+2Ag(NH3)2++2OH-![]() NH4++CO32-+2Ag↓+3NH3+H2O BCDE HCOOH+CH318OH
NH4++CO32-+2Ag↓+3NH3+H2O BCDE HCOOH+CH318OH![]() HCO18OCH3+H2O 乙 冷凝效果好,减少了甲醇等有毒物质对大气的污染 冷凝回流 除去甲酸,吸收乙醇,减少产物在水中的溶解度 分液漏斗 强碱性条件下,甲酸甲酯水解了
HCO18OCH3+H2O 乙 冷凝效果好,减少了甲醇等有毒物质对大气的污染 冷凝回流 除去甲酸,吸收乙醇,减少产物在水中的溶解度 分液漏斗 强碱性条件下,甲酸甲酯水解了
【解析】
(1)甲酸和氢氧化钠发生酸碱中和反应,生成相应的盐和水;
(2)能发生银镜反应的物质必含有醛基官能团,甲酸含有醛基,可以发生银镜反应;
(3)依据银镜反应的实验操作和注意问题分析判断;
(4)依据酯化反应的反应历程是羧酸脱羟基醇脱氢书写;
(5)根据甲醇性质分析,甲醇是有毒的易挥发的有机物;
(6)根据甲酸、甲醇的性质和饱和碳酸钠的作用解答;
(7)酯在碱溶液中水解生成羧酸盐和醇。
(1)甲酸与氢氧化钠溶液发生酸碱中和反应,生成甲酸钠和水,方程式为:NaOH+HCOOH=HCOONa+H2O;
(2)甲酸含有醛基,能发生银镜反应,发生反应HCOO-+2Ag(NH3)2++2OH-![]() NH4++CO32-+2Ag↓+3NH3+H2O;
NH4++CO32-+2Ag↓+3NH3+H2O;
(3)银镜反应的条件是在碱性条件下发生,在新制的银氨溶液中加入少量需要检验的有机物,水浴加热,生成银镜现象,反应过程中不能振荡,试管要洁净,银氨溶液需要新制,制备方法是想硝酸银溶液中加入氨水,生成沉淀,继续加入到沉淀恰好溶解得到银氨溶液,所以成功的做了银镜反应,
A.用洁净试管使银析出均匀,故A需要;
B.银镜反应需要反应的条件是碱性条件,不需要用硝酸酸化,故B不需要;
C.久置的银氨溶液会析出氮化银、亚氨基化银等爆炸性沉淀物,易发生危险。故C不需要;
D.银镜反应需要反应的条件是碱性条件,甲酸不能过量,故D不需要;
E.在浓度为2%的NH3H2O中滴入稍过量的浓度为2%的硝酸银,滴加试剂顺序错误,需碱过量,故E不需要;
故答案为:BCDE;
(4)甲酸和甲醇进行酯化反应的历程是羧酸脱羟基醇脱氢,反应化学方程式为:HCOOH+CH318OH![]() HCO18OCH3+H2O;
HCO18OCH3+H2O;
(5)甲醇是有毒的易挥发的有机物,需要密封装置中进行,所以选择乙,冷凝效果好,再加之乙装置中长导管C的冷凝回流作用,减少了甲醇等有毒物质对大气的污染;
(6)为了降低甲酸甲酯的溶解度,同时还能除去混有的甲醇和甲酸,需用饱和碳酸钠溶液;甲酸甲酯在饱和碳酸钠溶液中的溶解度极小,分离两种互不相溶的液体,用分液将其分离,分液用到分液漏斗;
(7)用装有饱和氢氧化钠的三颈瓶接收甲酸甲酯,几乎没有收集到产物,是因为甲酸甲酯在NaOH溶液中发生水解,生成甲酸钠和甲醇,得不到酯。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】某 500 mL 溶液中只可能含有 Na+、NH4+、Mg2+、Al3+、Fe2+、Fe3+、Cl-、![]() 、
、![]() 中 的几种离子。
中 的几种离子。
已知:NH4++OH-=NH3↑ +H2O
(1)取该溶液l00 mL,逐滴加入足量的NaOH溶液并加热,生成标准状况下的气体体积为 896 mL(气体已全部逸出),滴加过程中无沉淀生成。则该溶液中一定不含有的阳离子是______.
(2)另取100 mL原溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀6.27 g,再加入足量稀盐酸,沉淀部分溶解,生成标准状况下的气体体积为448 mL。则原浓液中下列离子的浓度:
离子种类 | 离子浓度 |
| ①___molL-1 |
| ②___ molL-1 |
Na+ | ③__molL-1 |
写出加入盐酸时,生成气体的离子方程式:__________。